Одноосновные карбоновые кислоты: свойства и номенклатура
Изучите структуру, гомологический ряд и физические свойства карбоновых кислот: от муравьиной до высших жирных кислот.
Одноосновные карбоновые кислоты
Номенклатура, изомерия и физические свойства
Определение
Насыщенные одноосновные карбоновые кислоты — это органические соединения, в молекулах которых одна карбоксильная группа (-COOH) связана с атомом водорода или алкильным радикалом. Общая формула ряда: CnH2n+1COOH.
Муравьиная кислота (HCOOH)
Первый представитель гомологического ряда. Бесцветная жидкость с резким запахом. Впервые выделена из лесных муравьев. Встречается в крапиве, хвое и выделениях медуз. Температура кипения 101 °C.
Уксусная кислота (CH3COOH)
Второй представитель ряда. Бесцветная жидкость с характерным резким запахом. Молекулы отличаются от муравьиной кислоты на одну группу CH2. Температура кипения 118 °C.
Высшие жирные кислоты
Имеют длинную цепь атомов углерода.
Пальмитиновая кислота: C15H31COOH (t пл. = 63 °C).
Стеариновая кислота: C17H35COOH (t пл. = 70 °C).
Твердые вещества, нерастворимые в воде, без запаха.
Названия кислот по систематической номенклатуре строятся из названия соответствующего алкана и окончания «-овая кислота».
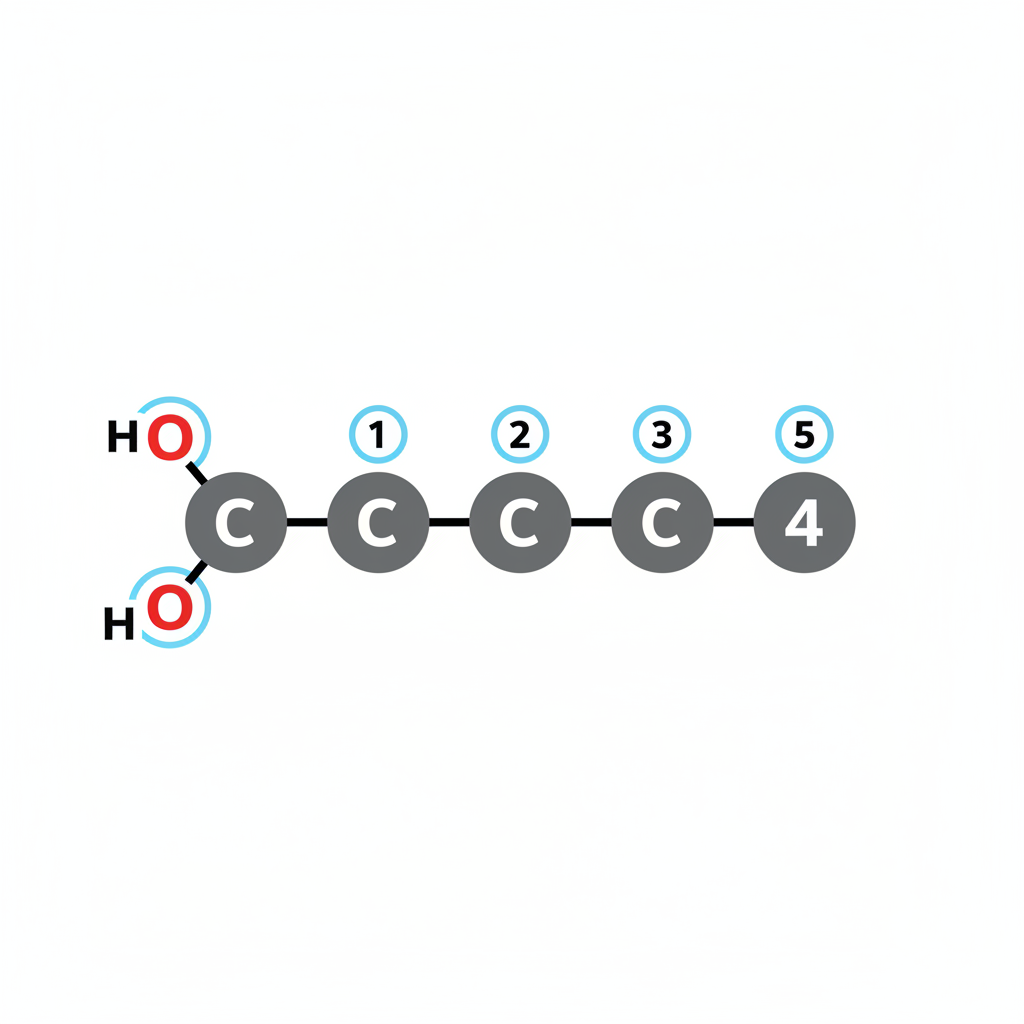
Правило номенклатуры ИЮПАК
Схематическая номенклатура
Нумерация начинается с атома углерода карбоксильной группы (C1). Например: H-COOH (метановая), CH3-COOH (этановая). При разветвленной цепи указывается положение радикалов.
Изомерия карбоновых кислот
Для карбоновых кислот возможна изомерия углеродного скелета.
Изомерия начинается с бутановой кислоты (C4).
Разветвленные изомеры: например, 2-метилпропановая кислота.
Изомерия положения группы -COOH невозможна, так как она всегда находится на конце цепи.
Температуры кипения кислот
С увеличением молекулярной массы температуры кипения закономерно возрастают. Они значительно выше, чем у спиртов и альдегидов.
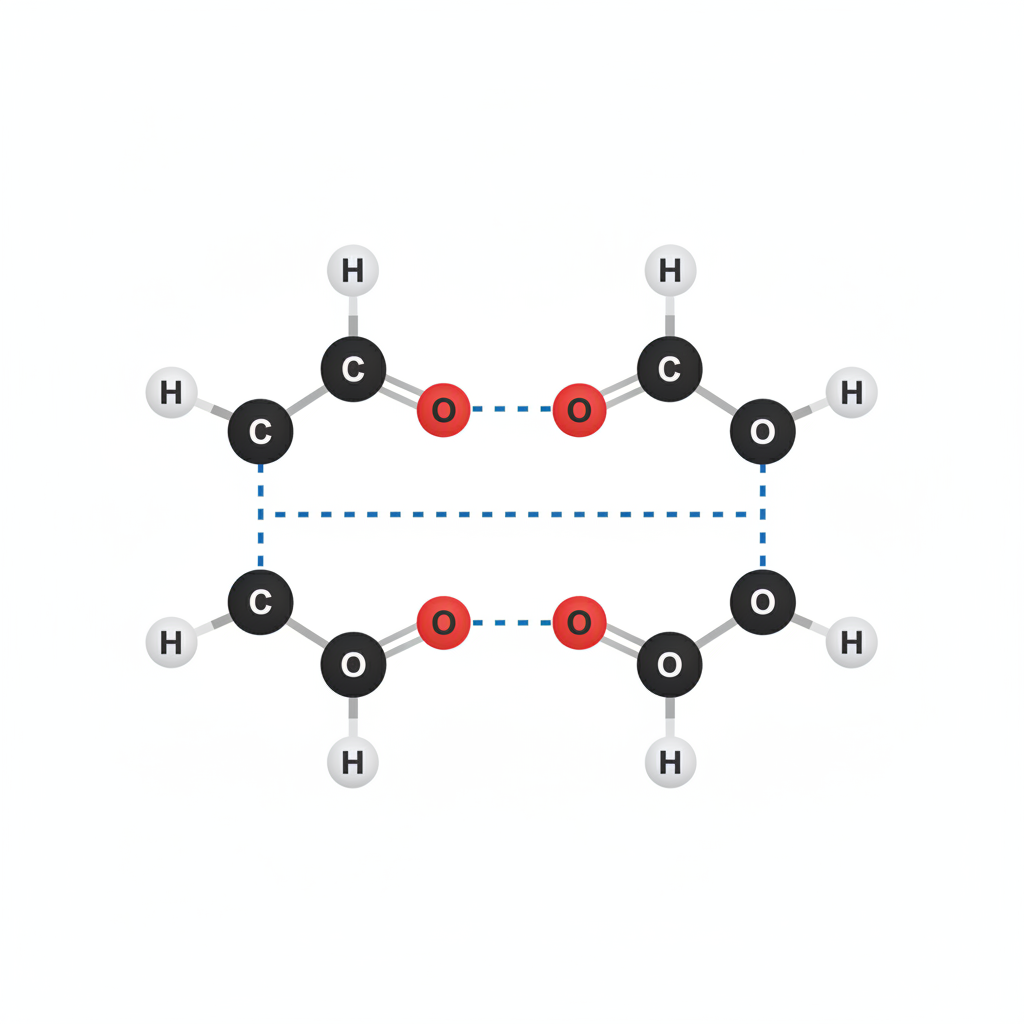
Водородные связи
Высокие температуры кипения объясняются образованием прочных водородных связей между молекулами кислот. Карбоновые кислоты часто существуют в виде димеров, где две молекулы связаны двумя водородными мостиками.
Растворимость в воде
Муравьиная, уксусная и пропановая кислоты смешиваются с водой в любых соотношениях.
С увеличением углеводородного радикала растворимость уменьшается.
Гидрофобный радикал препятствует растворению при росте цепи.
Высшие жирные кислоты (пальмитиновая, стеариновая) в воде не растворяются.
Сравнение с альдегидами
В отличие от альдегидов, среди карбоновых кислот нет газообразных веществ при комнатной температуре. Это результат более сильного межмолекулярного взаимодействия благодаря полярной группе -OH.
Шаростержневая модель пальмитиновой кислоты
Краткие итоги
Одноосновные кислоты имеют функциональную группу -COOH.
Простейшие представители — жидкости, высшие — твердые вещества.
Наличие водородных связей обеспечивает высокие температуры кипения.
Растворимость в воде падает с ростом молекулярной массы.
Спасибо за внимание!
Химия — 10 класс
- химия
- карбоновые-кислоты
- органическая-химия
- уксусная-кислота
- номенклатура-июпак
- водородные-связи