Das Bohrsche Atommodell: Postulate und Quantensprünge
Lernen Sie die Grundlagen des Bohrschen Atommodells kennen: Von Niels Bohrs Postulaten bis zum Wasserstoffspektrum und den Grenzen der Theorie.
Das Bohrsche<br>Atommodell
Wie Niels Bohr das Atom verstand
Podcast-Begleitpräsentation
Niels Bohr –<br>Der Mann hinter dem Modell
Geboren 1885 in Kopenhagen
Studium der Physik, Promotion 1911
Arbeit bei Rutherford in Manchester
1913: Veröffentlichung des Atommodells
1922: Nobelpreis für Physik
Atommodelle vor Bohr
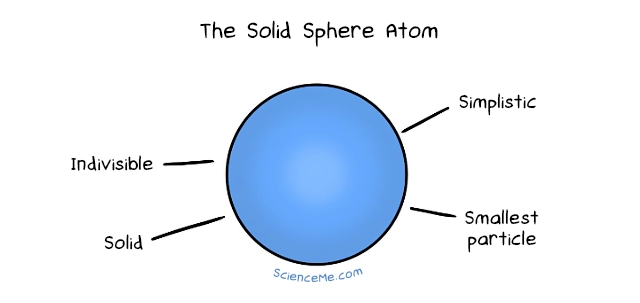
Dalton (1803)
Atom als unteilbare Kugel
Thomson (1897)
Rosinenkuchen-Modell,<br>Elektronen eingebettet
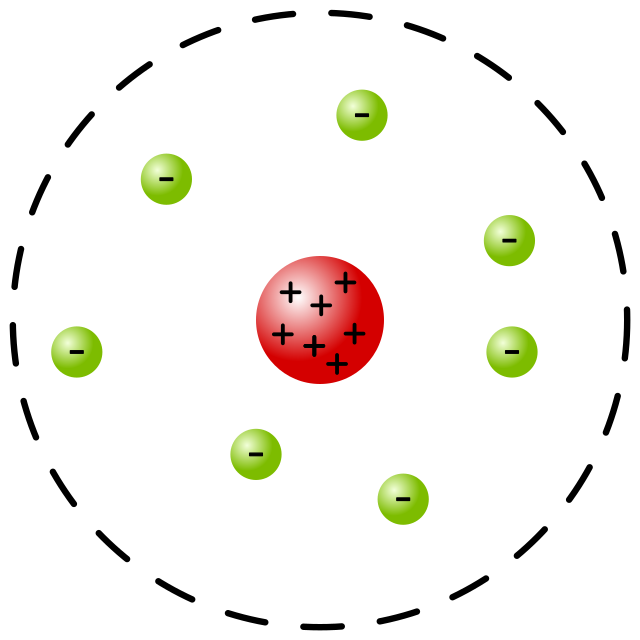
Rutherford (1911)
Kern-Hülle-Modell,<br>Elektronen kreisen frei
Die 3 Postulate Bohrs
<svg xmlns="http://www.w3.org/2000/svg" viewBox="0 0 24 24" width="80" height="80"><defs><filter id="glowOrbit"><feGaussianBlur stdDeviation="1.5" result="coloredBlur"/><feMerge><feMergeNode in="coloredBlur"/><feMergeNode in="SourceGraphic"/></feMerge></filter></defs><g fill="none" stroke="#00e5ff" stroke-width="1.5" stroke-linecap="round" stroke-linejoin="round" filter="url(#glowOrbit)"><circle cx="12" cy="12" r="2.5" fill="#00e5ff" /><ellipse cx="12" cy="12" rx="9" ry="3" transform="rotate(45 12 12)" /><ellipse cx="12" cy="12" rx="9" ry="3" transform="rotate(-45 12 12)" /><circle cx="6" cy="6" r="1.5" fill="#00e5ff" stroke="none" /></g></svg>
<svg xmlns="http://www.w3.org/2000/svg" viewBox="0 0 24 24" width="80" height="80"><defs><filter id="glowWave"><feGaussianBlur stdDeviation="1.5" result="coloredBlur"/><feMerge><feMergeNode in="coloredBlur"/><feMergeNode in="SourceGraphic"/></feMerge></filter></defs><g fill="none" stroke="#00e5ff" stroke-width="2" stroke-linecap="round" stroke-linejoin="round" filter="url(#glowWave)"><path d="M2 12 Q 7 2, 12 12 T 22 12" /></g></svg>
<svg xmlns="http://www.w3.org/2000/svg" viewBox="0 0 24 24" width="80" height="80"><defs><filter id="glowPhoton"><feGaussianBlur stdDeviation="1.5" result="coloredBlur"/><feMerge><feMergeNode in="coloredBlur"/><feMergeNode in="SourceGraphic"/></feMerge></filter></defs><g fill="none" stroke="#00e5ff" stroke-width="2" stroke-linecap="round" stroke-linejoin="round" filter="url(#glowPhoton)"><circle cx="12" cy="12" r="3" fill="#00e5ff" /><line x1="12" y1="3" x2="12" y2="6" /><line x1="12" y1="18" x2="12" y2="21" /><line x1="5.64" y1="5.64" x2="7.76" y2="7.76" /><line x1="16.24" y1="16.24" x2="18.36" y2="18.36" /><line x1="3" y1="12" x2="6" y2="12" /><line x1="18" y1="12" x2="21" y2="12" /><line x1="5.64" y1="18.36" x2="7.76" y2="16.24" /><line x1="16.24" y1="7.76" x2="18.36" y2="5.64" /></g></svg>
Elektronen bewegen sich auf <span style="color: #00e5ff; font-weight: 500;">festen Kreisbahnen (Schalen)</span> um den Kern
Auf diesen Bahnen strahlen Elektronen <span style="color: #00e5ff; font-weight: 500;">keine Energie</span> ab
Beim <span style="color: #00e5ff; font-weight: 500;">Sprung zwischen Bahnen</span> wird Energie als Licht emittiert oder absorbiert
Der Quantensprung
Energie wird als Licht (Photon) abgegeben, wenn ein Elektron von einer höheren auf eine niedrigere Schale springt.
E = h · f
Plancksche Relation
n=1
n=2
n=3
n=4
Podcast-Begleitpräsentation
Das Wasserstoffspektrum
Jede Spektrallinie entspricht einem bestimmten Quantensprung.
Lyman-Serie
Ultravioletter Bereich (UV)
Balmer-Serie
Sichtbarer Bereich
Paschen-Serie
Infraroter Bereich
Grenzen des Modells
Schwächen des Modells
Nur für Wasserstoff exakt gültig
Keine Erklärung der Linienintensitäten
Widerspricht klassischer Physik
Elektronen sind keine Teilchen auf Bahnen (Quantenmechanik)
Was Bohr richtig lag:
Quantisierte Energieniveaus
Grundprinzip des Energiesprungs
Basis für die moderne Quantenmechanik
Fazit
Jeder, der nicht schockiert ist von der Quantenmechanik, hat sie nicht verstanden.
Niels Bohr
Bohrs Modell war revolutionär – ein erster Schritt in die Welt der Quantenphysik.
Danke fürs Zuhören! 🎙️
- atommodell
- niels bohr
- physik
- quantenphysik
- chemie
- wasserstoffspektrum
- wissenschaft