Arzneimittelchemie: Entwicklung, Struktur und Wirkung
Lernen Sie die Grundlagen der Arzneimittelchemie: Von funktionellen Gruppen und Stereochemie bis zur Synthese von Aspirin und Wirkmechanismen.
Arzneimittelchemie
Entwicklung und Wirkung von Arzneimitteln
Nicolai Kaiser
Gliederung
Einleitung & Geschichte der Arzneimittelchemie
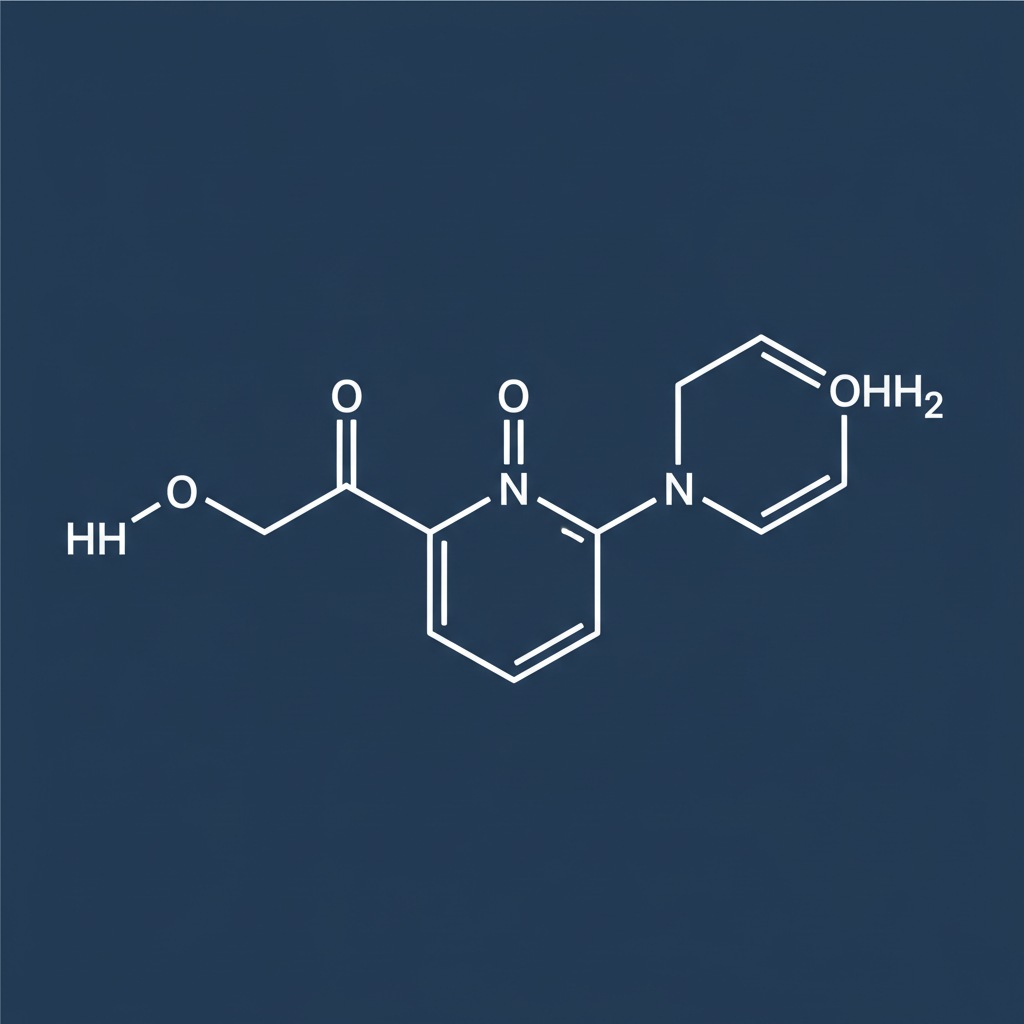
Chemische Grundlagen & funktionelle Gruppen
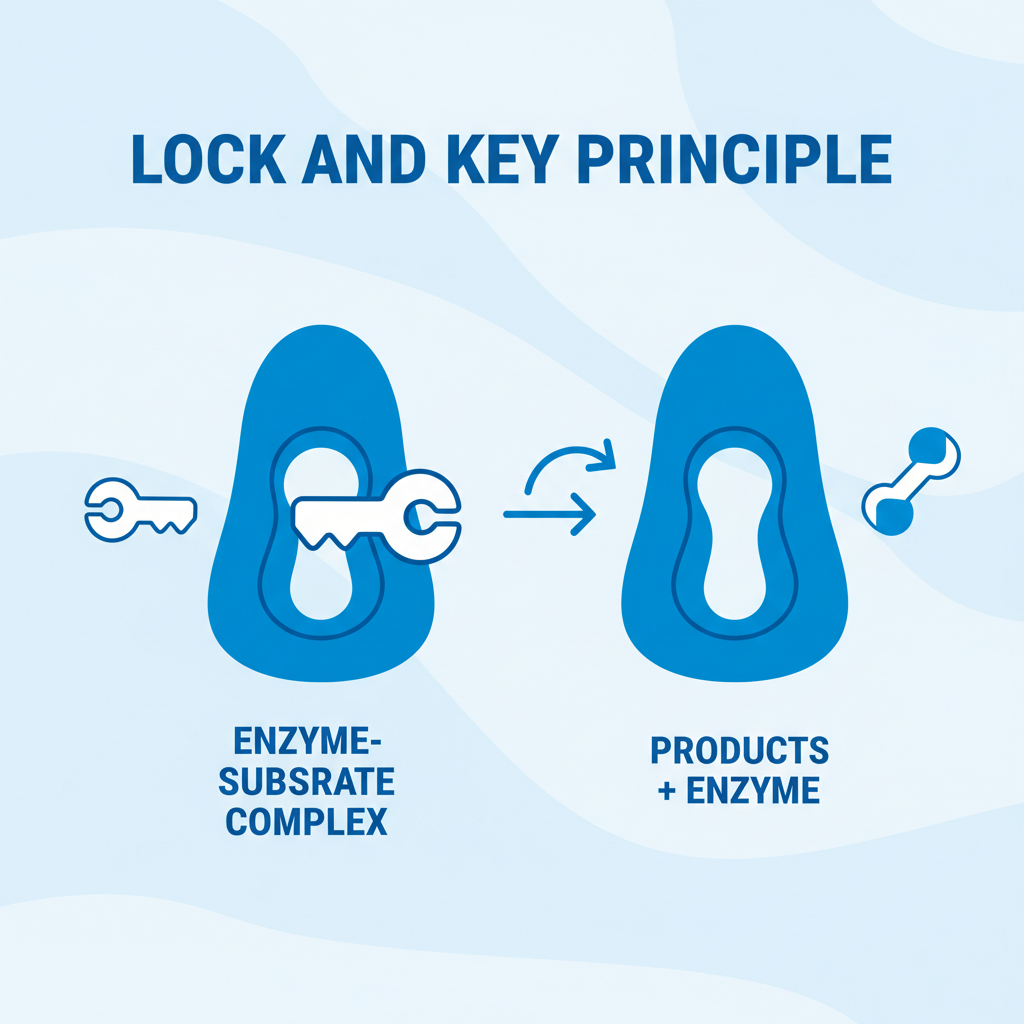
Wechselwirkungen mit Zielproteinen
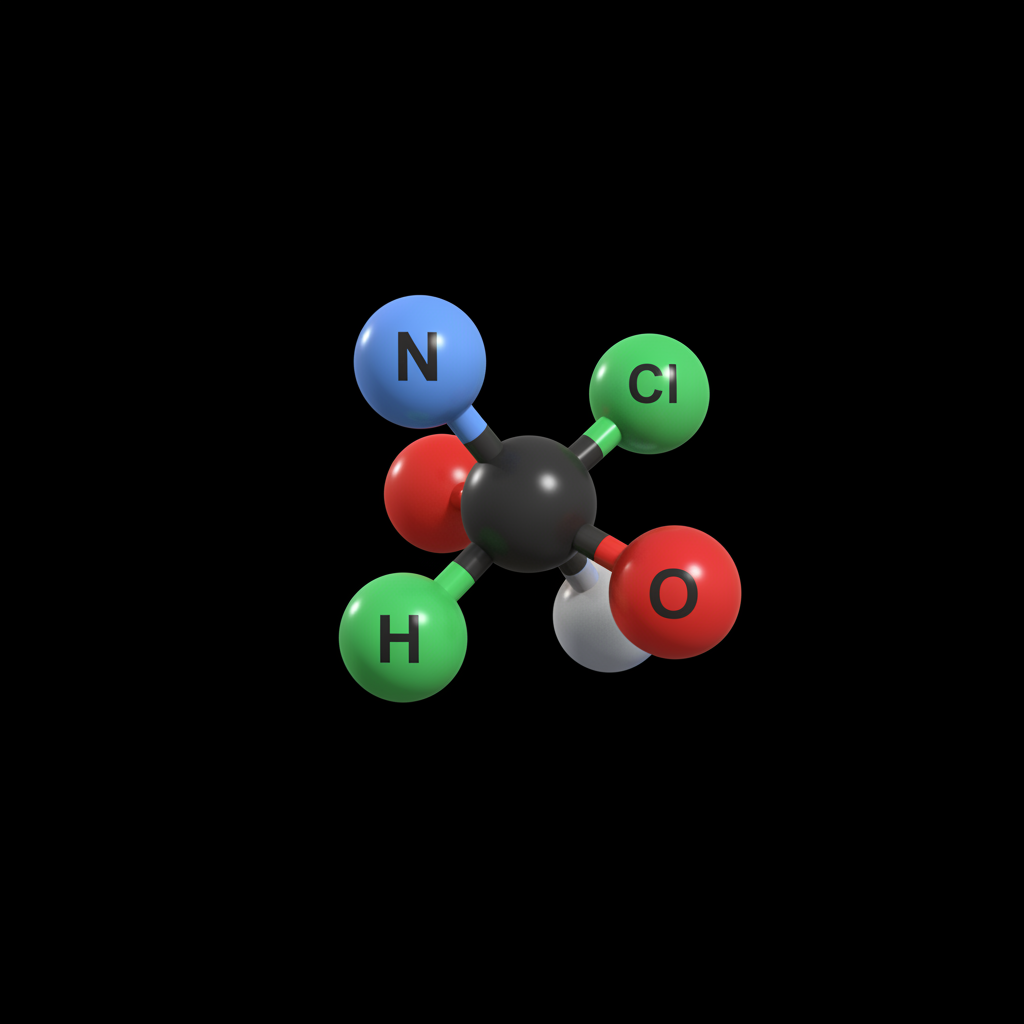
Stereochemie & Chiralität
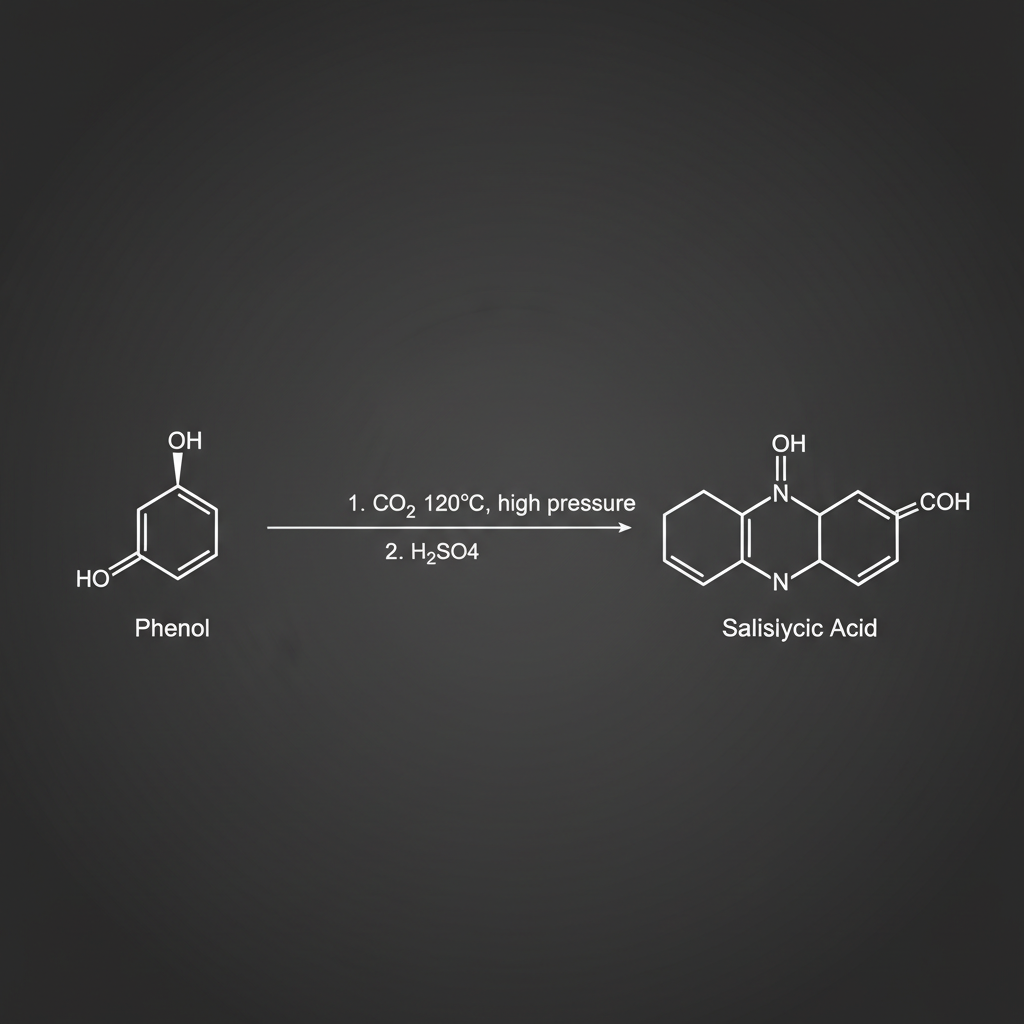
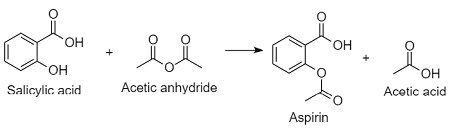
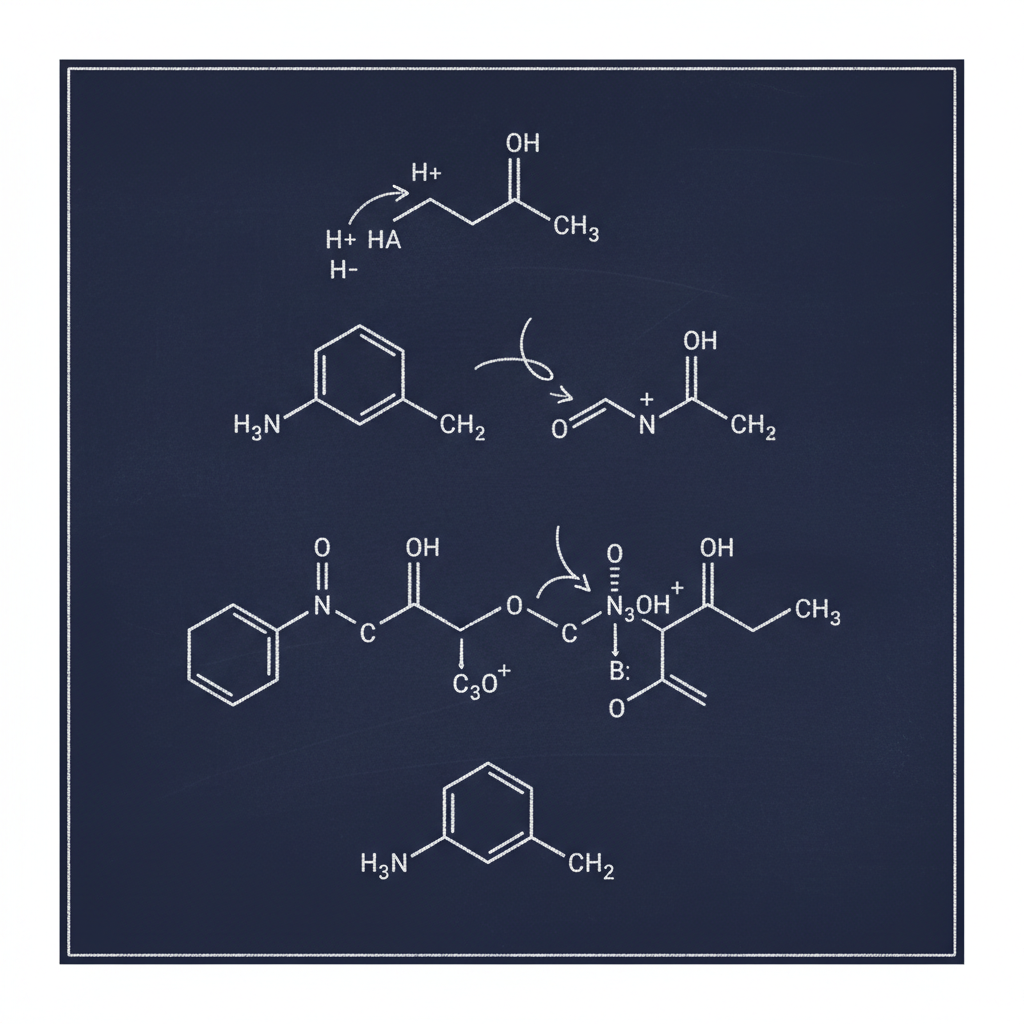
Synthese & Reaktionsmechanismen (Aspirin)
Einleitung – Vom Pflanzenextrakt zum Molekül
- arzneimittelchemie
- chemie
- pharmazie
- aspirin-synthese
- stereochemie
- wirkstoffdesign
- biochemie