Neuroprotection : Phénylbutyrate et Encéphalopathie Prématurée
Étude du Phénylbutyrate de Sodium (PBA) sur la substance blanche et le neurodéveloppement dans un modèle murin d'encéphalopathie de la prématurité.
Effets du Phénylbutyrate de Sodium (PBA) dans un Modèle Murin d'Encéphalopathie de la Prématurité
Impact sur la Substance Blanche et le Neurodéveloppement
M.-A. Le Ray, C. Larralde, S. Marret, B.J. Gonzalez, C. Cleren, et al.
I. Contexte Clinique : Encéphalopathie de la Prématurité
Incidence élevée : 20 pour 1000 naissances vivantes. Risque majeur de troubles neurodéveloppementaux.
Évolution des lésions : Diminution des lésions kystiques sévères au profit de lésions diffuses de la substance blanche (WMI).
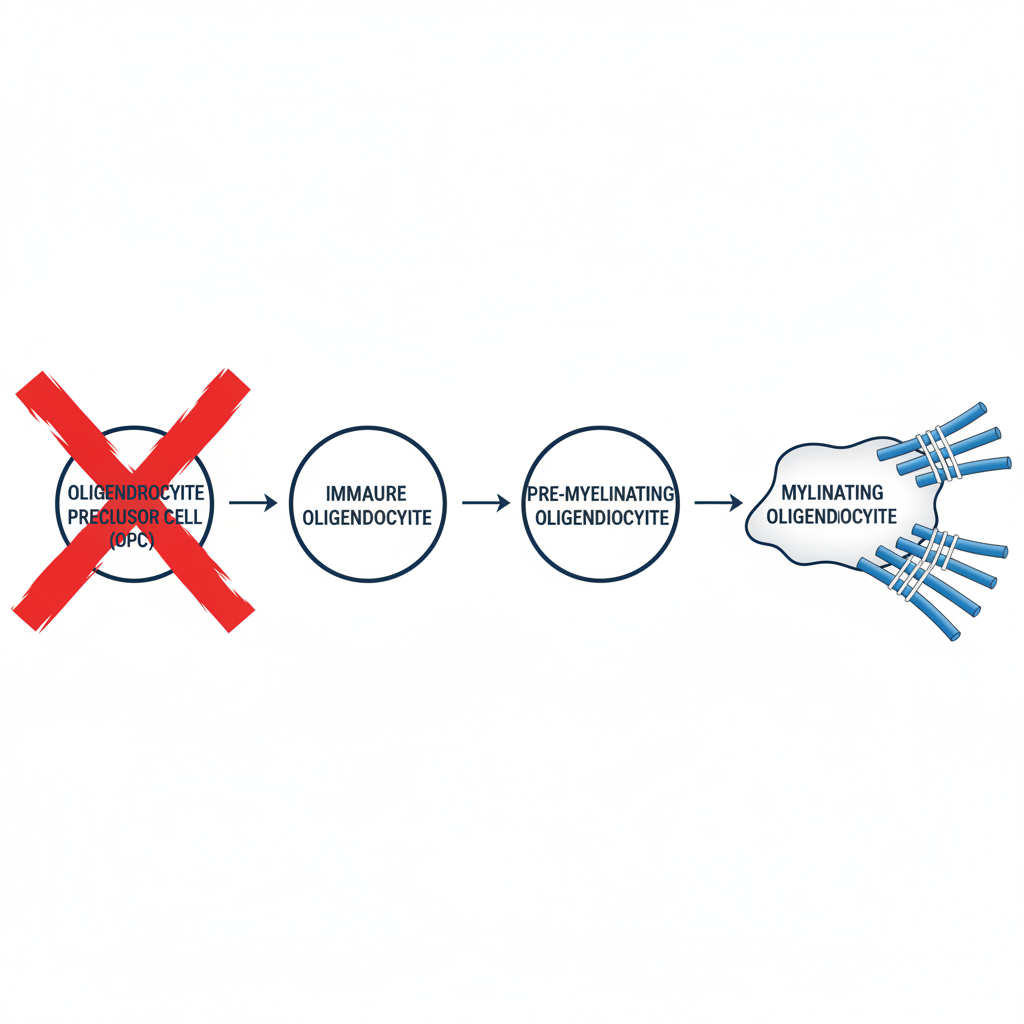
Mécanisme : Mort sélective des précurseurs d'oligodendrocytes (Pre-OL) et astrocytes entraînant une hypomyélinisation.
Vulnérabilité de la Substance Blanche (24-32 SA)
Fenêtre critique : Maturation des oligodendrocytes très sensible à l'hypoxie/inflammation.
Conséquences : Défaut de maturation (arrêt de différenciation) sans mort cellulaire massive.
Séquelles : Déficits moteurs (diplégie spastique) et cognitifs persistants.
II. Le Rationnel du Modèle JH (Jugular Hypoxia)
Un modèle mimant les complications des soins intensifs néonataux (cathéters veineux centraux).
Souris P5 : Équivalent humain grand prématuré (24-32 SA).
Procédure : Ligature veine jugulaire externe gauche + Hypoxie (8% O2, 45 min).
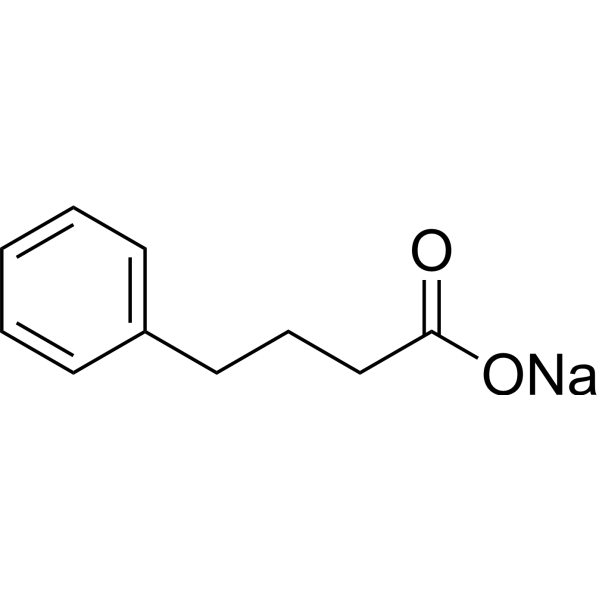
Stratégie Thérapeutique : Phénylbutyrate de Sodium (PBA)
Molécule déjà approuvée (traitement des troubles du cycle de l'urée).
Mécanismes potentiels : Chaperon chimique (réduit stress du réticulum endoplasmique), inhibiteur d'HDAC (épigénétique).
Objectif : Prévenir les lésions de la substance blanche et les déficits comportementaux induits par le modèle JH.
III. Matériel et Méthodes : Design Expérimental
4 Groupes : Sham-PBS, Sham-PBA, JH-PBS, JH-PBA (Mâles & Femelles)
Analyses : Histologie (PDGFRa, MBP, TTC) & Comportement (Moteur, Social, Cognitif)
IV. Résultats I : Atteintes Histologiques (Court Terme P6)
Striatum (Mâles) : Augmentation significative (+34%) des précurseurs d'oligodendrocytes (PDGFRa+). Suggère un blocage de différenciation post-lésionnel. Le PBA ne corrige pas totalement cet effet.
Viabilité Tissulaire (TTC P10) : Effet du PBA
Le modèle JH induit une lésion tissulaire modérée (infarctus) visible à P10.
Le traitement PBA réduit la taille de la lésion de 43% (tendance favorable, p=0.42).
IV. Résultats I : Atteintes Histologiques (Long Terme P45)
Déficit de Myélinisation dans le Striatum (Sex-dependent)
Pas d'altération majeure dans le Corps Calleux.
Striatum Ventral (Mâles) : Réduction significative de 52% de la densité des fibres myélinisées (MBP).
Le PBA ne permet pas de restaurer significativement la densité de myéline chez les mâles.
V. Résultats II : Phénotypage Comportemental (Court Terme P6-P10)
Réflexe d'Agrippement (Grasping)
Déficit JH : -50% à -64% (Pattes arrières).
Effet PBA : Prévention quasi-totale des déficits.
Aversion du Vide (Cliff Aversion)
Déficit JH : +108% de temps pour se détourner.
Effet PBA : Retour aux valeurs contrôles.
V. Résultats II : Comportement Long Terme (Balance Beam)
Test de motricité fine et coordination sur poutre (P32).
JH augmente significativement le nombre de déséquilibres.
PBA prévient totalement ces déficits moteurs (p=0.02 vs JH-PBS).
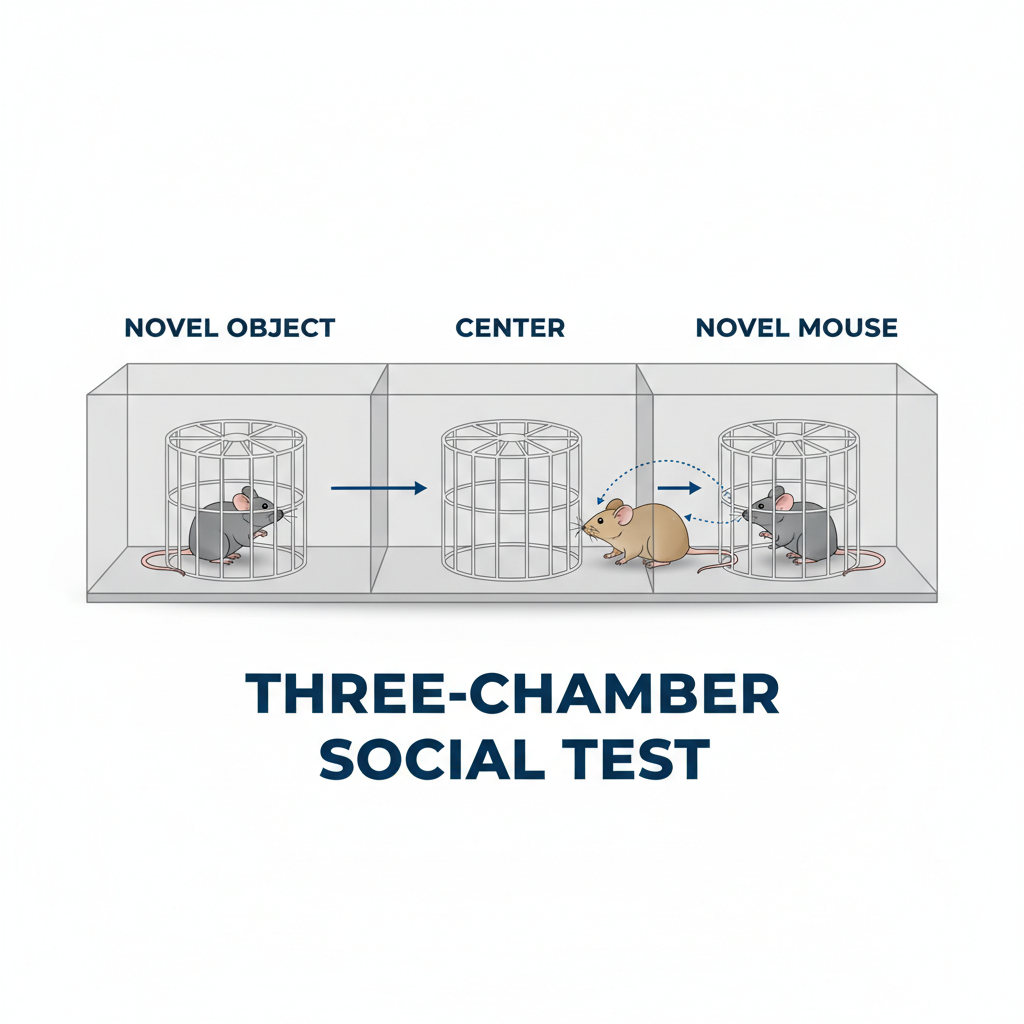
Résultats : Comportement Social & Cognitif
Mémoire Sociale (P30-31) : Les souris JH-PBA interagissent davantage avec la souris étrangère ('Stranger 2') que les souris JH-PBS.
Reconnaissance d'Objet (NOR P34) : Pas de déficit majeur observé chez les souris JH, ni d'effet délétère du PBA.
VI. Discussion : Le Paradoxe Histologie vs Comportement
Histologie Mitigée
Pas de restauration complète de la myéline (MBP) et persistance des défauts de précurseurs (PDGFRa) chez les mâles.
Succès Comportemental
Prévention totale des déficits moteurs (Grasping, Poutre) et sociaux.
Comment expliquer cette divergence ?
Hypothèse : Compensation et Plasticité
Plasticité Cérébrale : Réorganisation des réseaux neuronaux pour compenser la perte de myéline locale.
Stratégies Motrices : Les souris adoptent de nouvelles stratégies (ex: enrouler la queue autour de la poutre) pour réussir les tests.
Rôle du PBA : Action neuroprotectrice via régulation épigénétique (HDACi) favorisant l'adaptation neuronale plutôt que la réparation structurelle brute.
VII. Conclusions
Modèle Pertinent : JH reproduit une atteinte modérée (WMI) de type hypomyélinisation, avec dimorphisme sexuel (Mâles > Femelles).
Efficacité du PBA : Neuroprotection fonctionnelle majeure (moteur & social) à court et long terme.
Mécanisme : Discrépance histo-comportementale suggérant des mécanismes de compensation puissants induits par le PBA.
Perspectives
Exploration mécanistique : Analyse omique spatiale pour identifier les cibles moléculaires du PBA.
Thérapies combinées : Associer PBA avec une molécule pro-myélinisante ?
Étude du Sexe : Comprendre la résilience naturelle des femelles dans ce modèle.
- neuroprotection
- prématurité
- substance-blanche
- pba
- neurosciences
- modèle-murin
- recherche-médicale