Uch Tomonlama Kimyoviy Bog'lanish: Sigma va Pi Bog'lari
Uch tomonlama bog'lanish, sp gibridlanish, sigma va pi bog'larning tuzilishi hamda azot va asetilen kabi misollar haqida batafsil ma'lumot.
Uch tomonlama bog'lanish
Kimyoviy bog'lanish turlari | Triple Bond
Kimyo Fanlari
Kimyoviy bog'lanish nima?
Kirish
Kimyoviy bog'lanish — atomlar orasidagi elektron juftlari orqali hosil bo'ladigan kuch bo'lib, molekulalar va kristallar tarkibini birlashtiradi.
Yakka bog'lanish
σ (sigma) bog'
Qo'shaloq bog'lanish
1σ + 1π bog'
Uch tomonlama bog'lanish
1σ + 2π bog'
H₂ (Yakka bog')
O₂ (Qo'shaloq bog')
N₂ (Uch tomonlama bog')
Uch tomonlama bog'lanish ta'rifi
Kimyoviy Bog'lanish
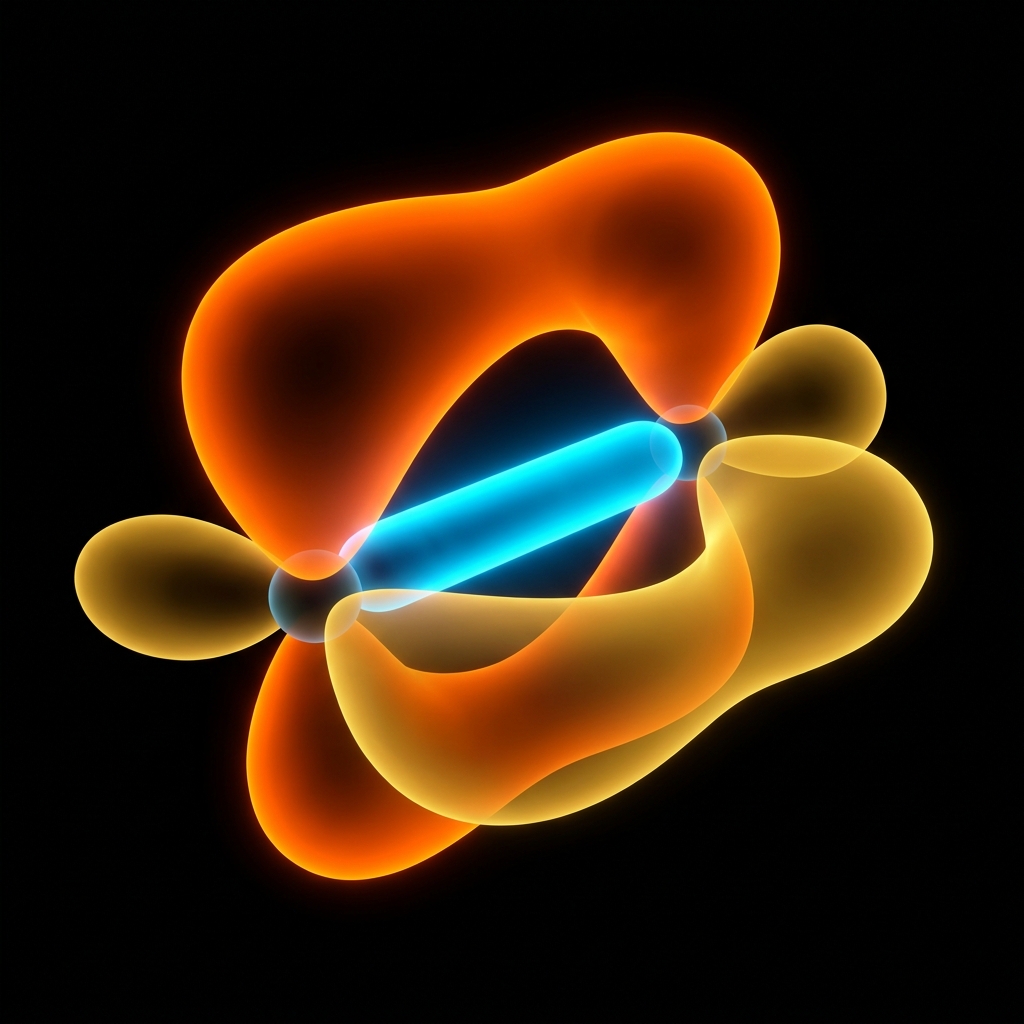
<b style="color:#ffffff;">Uch tomonlama bog'lanish</b> — ikki atom o'rtasida <b>uchta umumiy elektron juftidan</b> iborat kimyoviy bog'lanish bo'lib, bitta <b style="color:#5ce1e6;">σ (sigma)</b> va ikkita <b style="color:#ff3366;">π (pi)</b> bog'dan tashkil topadi.
<b>1 ta σ</b> bog' <br><span style="color:#8a9fb5; font-size:16px;">va</span> <b>2 ta π</b> bog'
<b>3</b> <br><span style="color:#8a9fb5; font-size:14px; font-weight:400; line-height:1.2; display:block; margin-top:2px;">(uchta elektron juft qatnashadi)</span>
Eng <b>kuchli</b> va eng <b>qisqa</b> <br><span style="color:#8a9fb5; font-size:16px; font-weight:400;">kovalent bog' turi</span>
Energiyasi: <span style="color:#ffaa00;">~837 kJ/mol</span><br>Uzunligi: <span style="color:#ffaa00;">~120 pm</span>
N≡N (Azot molekulasi) orbital tuzilishi
KIMYONING ASOSLARI
σ va π bog'larning tuzilishi
σ (Sigma) bog'
π (Pi) bog' (x2)
Ikki atomning orbital o'qlari bo'ylab to'g'ridan-to'g'ri o'zaro ta'sir
Kuchli va simmetrik markazga ega
Aylanish erkin bo'lib, energiya talab qilmaydi
Orbital o'qlarga perpendikulyar yo'nalishda ta'sir ko'rsatadi
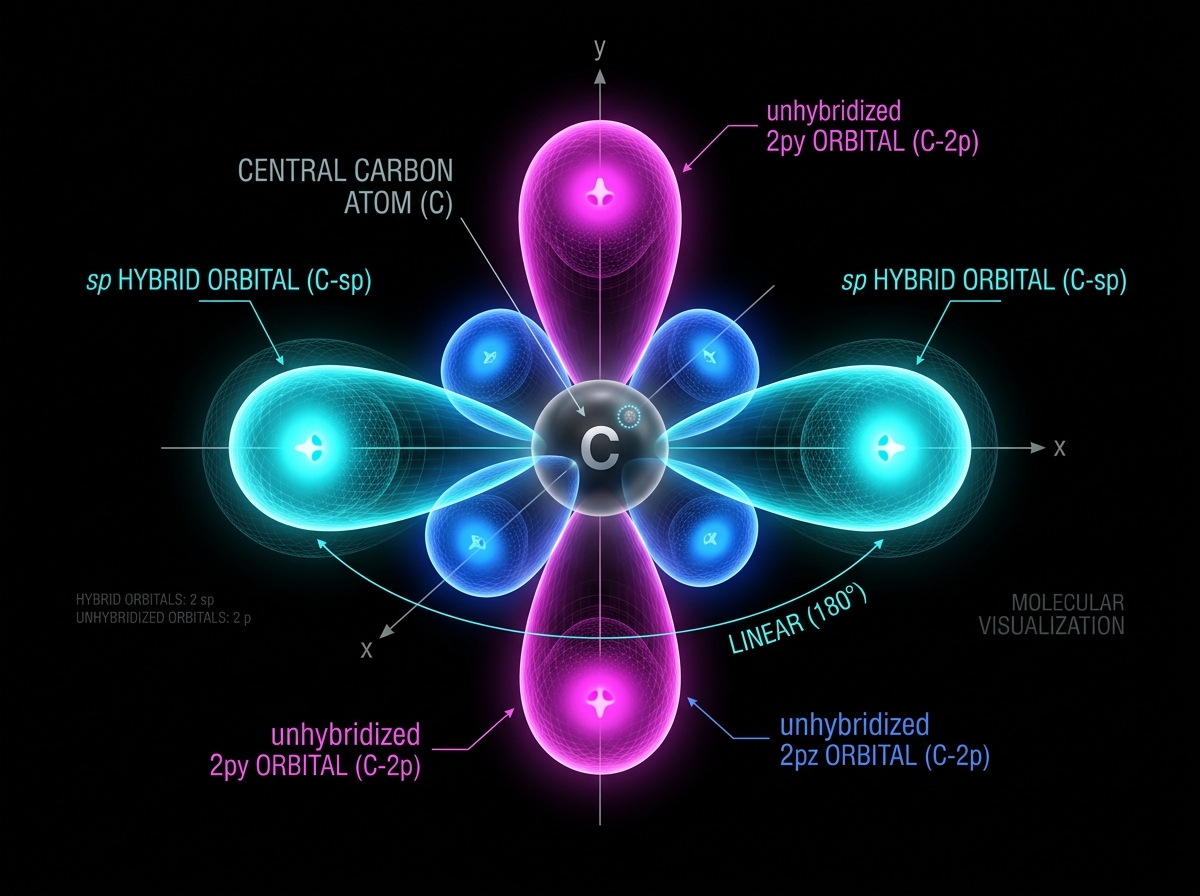
sp gibridlanish natijasida hosil bo'ladi
Ikkita parallel π bulut mavjud
sp Gibridlanish
Uch tomonlama bog'lanish sp gibridlanish natijasida hosil bo'ladi
Uch tomonlama bog'lanish
Uch tomonlama bog'lanish misollari
Kimyoviy bog'lanishlar
Bog' turlarini solishtirish
Yakka, Qo'shaloq va Uch tomonlama bog'lar
KIMYO FANLARI
Kimyo Fanlari
Uch tomonlama bog'lanishning xossalari
🔗
Bog' kuchi
Eng kuchli kovalent bog' turi. N≡N: 945 kJ/mol
📏
Bog' uzunligi
Eng qisqa bog'. C≡C: ~120 pm
⚡
Reaktivlik
π bog'lar tufayli kimyoviy reaktsiyalarga moyil
📐
Molekula shakli
sp gibridlanish → chiziqli geometriya (180°)
⚖️
Bog' tartibi
Bond order = 3, elektronlar zichligi yuqori
🧲
Qutblilik
Turli atomlar orasida qutbli bo'lishi mumkin (C≡O, H-C≡N)
Amaliy qo'llanilishi
Uch Tomonlama Bog'lanish
Xulosa
Uch tomonlama bog'lanish: 1σ + 2π bog'dan iborat
sp gibridlanish natijasida hosil bo'ladi (180° burchak)
Eng qisqa va eng kuchli kovalent bog' turi
Asosiy misollar: N₂, C₂H₂, CO, HCN
Sanoat, qishloq xo'jaligi va farmatsevtikada keng qo'llaniladi
1σ + 2π
BOG' TURI
3
BOG' TARTIBI
~837-945 kJ/mol
ENERGIYA
110-121 pm
UZUNLIK
Kimyo | Uch tomonlama bog'lanish
- kimyo
- uch-tomonlama-bog'lanish
- sigma-bog'
- pi-bog'
- sp-gibridlanish
- azot
- atsetilen
- molekulyar-geometriya