Électrodéposition et Oxydoréduction : Cours de Chimie
Découvrez les principes de la galvanisation, de la restauration par électrolyse et l'analogie redox avec la photosynthèse. Cours complet de chimie.
Électrodéposition et Oxydoréduction : De la Galvanisation à la Photosynthèse
Cours : Chimie des solutions 202-SN2-T2
Collège Laflèche – Sciences de la nature
Membres de l'équipe : [Noms des coéquipiers]
Avril 2026
Protection du Clou — Galvanisation
Processus
Dépôt de zinc sur un clou en fer pour le protéger de la corrosion
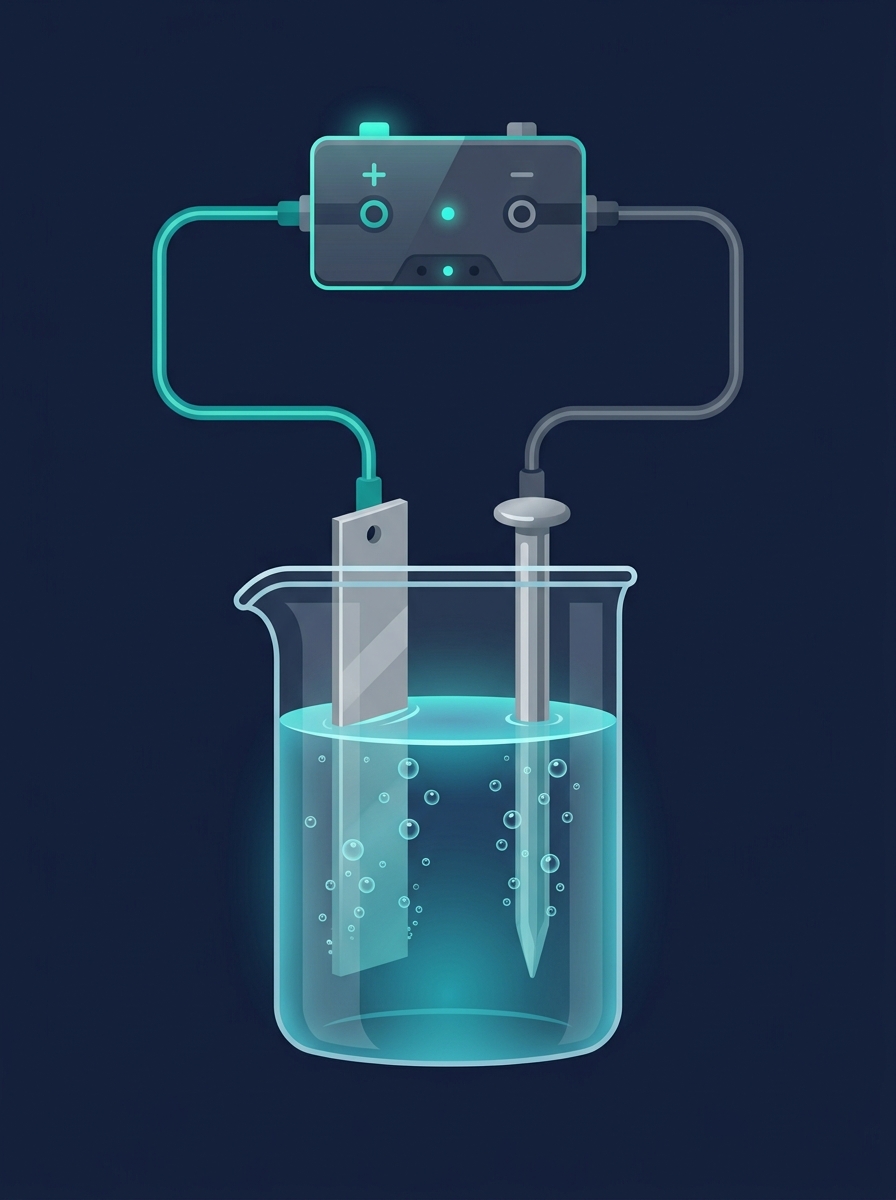
Composants du montage
Source de tension (bloc d'alimentation)
Anode : clou sacrificiel (se dissout)
Cathode : clou à protéger (reçoit le dépôt)
Fils conducteurs
Électrolyte : ZnCl₂ et HCl
Sens des électrons
De l'anode (+) → vers la cathode (−)
Anode (Fer)
Cathode (Zinc)
ZnCl₂ / HCl
e⁻ →
Chimie des solutions 202-SN2-T2 | Collège Laflèche
Réactions à l'Œuvre — Électrodéposition
Électrode
Réaction Balancée
Type
Anode (Fer)
Fe(s) → Fe²⁺(aq) + 2e⁻
Oxydation
Cathode (Zinc)
Zn²⁺(aq) + 2e⁻ → Zn(s)
Réduction
États d'Oxydation
Fe : 0 → +2 (Oxydation)
Zn : +2 → 0 (Réduction)
Fournisseur d'électrons
Le clou en fer (Anode)
Type de cellule
Électrolytique (non spontanée)
Chimie des solutions 202-SN2-T2 | Collège Laflèche
Variations de Masse et de Concentration
Variations de Masse
Variations de Concentration
Rôle du Bloc d'Alimentation
CHIMIE DES SOLUTIONS 202-SN2-T2 | COLLÈGE LAFLÈCHE
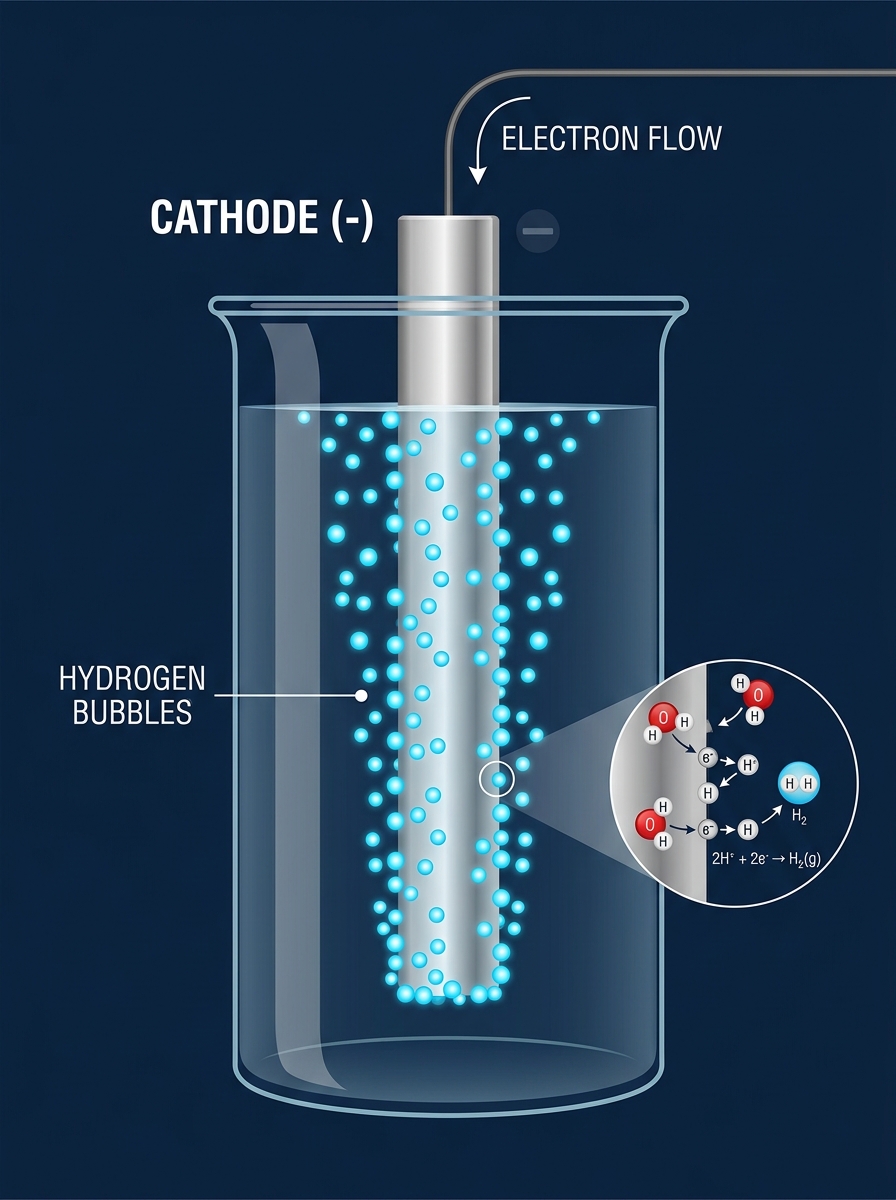
Réaction Nuisible et Rendement
Réaction parasite à la cathode:
2H⁺(aq) + 2e⁻ → H₂(g)
Effets Néfastes
Baisse du rendement : consommation d'électrons destinés au zinc
Dépôt non uniforme : bulles de H₂ créent des irrégularités à la surface
Le zinc ne se dépose pas correctement là où il y a des bulles
Conséquence sur le pH
Les ions H⁺ sont consommés → pH de la solution augmente progressivement
pH <span style="color: #ef4444; font-weight: bold;">↑</span> au fil de l'électrolyse
Chimie des solutions 202-SN2-T2 | Collège Laflèche
Restauration du Clou Rouillé
Principe & Fonctionnement
Électrolyse en milieu basique (NaHCO₃)
La cathode (clou rouillé) est inondée d'électrons
Les électrons réduisent les oxydes de fer (rouille)
Réaction : Fe₂O₃ + électrons → Fe (métal)
Milieu basique : solution de bicarbonate de soude
Montage
Similaire à l'électrodéposition
Clou sacrificiel à l'anode (protège la pièce principale)
Cathode = clou rouillé à restaurer
Électrolyte : NaHCO₃(aq)
Processus de Restauration
Avant
Après
Chimie des solutions 202-SN2-T2
Collège Laflèche
Transformations et Observations
Formation abondante de bulles de H₂ à la cathode
La rouille orange devient noire → Magnétite (Fe₃O₄)
Détachement des écailles de rouille grâce à la pression du gaz H₂
La solution devient brunâtre
Précipitation de l'hydroxyde de fer
Fe²⁺(aq) + 2OH⁻(aq) → Fe(OH)₂(s)
Précipité brun
La magnétite (Fe₃O₄) est la forme noire et magnétique de l'oxyde de fer — plus stable que la rouille
Chimie des solutions 202-SN2-T2 | Collège Laflèche
Analyse des Masses — Restauration
Cathode : Clou Rouillé
PERD DE LA MASSE
Élimination de la couche de rouille superficielle
La rouille (Fe₂O₃, Fe₃O₄) est réduite
Les oxydes sont éliminés ou se détachent
La masse du métal pur diminue légèrement
Anode : Clou Sacrificiel
PERD DE LA MASSE
Oxydation du fer métallique → ions Fe²⁺ en solution
Fe(s) → Fe²⁺(aq) + 2e⁻
Le métal se dissout progressivement
Perte de masse mesurable
Les deux électrodes subissent une diminution de masse — contrairement à l'électrodéposition où la cathode en gagne
Chimie des solutions 202-SN2-T2
Collège Laflèche
La Photosynthèse sous l'Angle Redox
Réduction du Carbone (C)
Oxydation de l'Oxygène (O)
Chimie des solutions 202-SN2-T2 | Collège Laflèche
Analyse Finale — Photochimie et Conclusion
Oxydant
CO₂
Accepte les électrons
C : +4 → 0 (se réduit)
Réducteur
H₂O
Fournit les électrons
O : −2 → 0 (s'oxyde)
Source d'Énergie
☀ Lumière solaire
Joue le rôle du bloc d'alimentation
Excite les électrons pour rendre la réaction possible
ANALOGIE : ÉLECTROLYSE VS PHOTOSYNTHÈSE
Bloc d'alimentation
Lumière solaire
Électrolyte
Chloroplastes
Électrodes
Molécules biologiques
La photosynthèse est une réaction d'oxydoréduction biologique non spontanée, rendue possible par l'énergie lumineuse — tout comme l'électrolyse est rendue possible par le courant électrique.
Chimie des solutions 202-SN2-T2
Collège Laflèche
- chimie
- oxydoréduction
- électrolyse
- galvanisation
- photosynthèse
- sciences
- électrodéposition