Salze in der Chemie: Eigenschaften & Beispiele (Klasse 8)
Lerne alles über Salze: Ionengitter, elektrische Leitfähigkeit, Neutralisation und Beispiele wie NaCl. Perfekt für den Chemieunterricht der 8. Klasse.
Salze in der Chemie
Vom Kochsalz bis zum Kristallgitter – Eine Reise in die Welt der Ionen
Was sind Salze eigentlich?
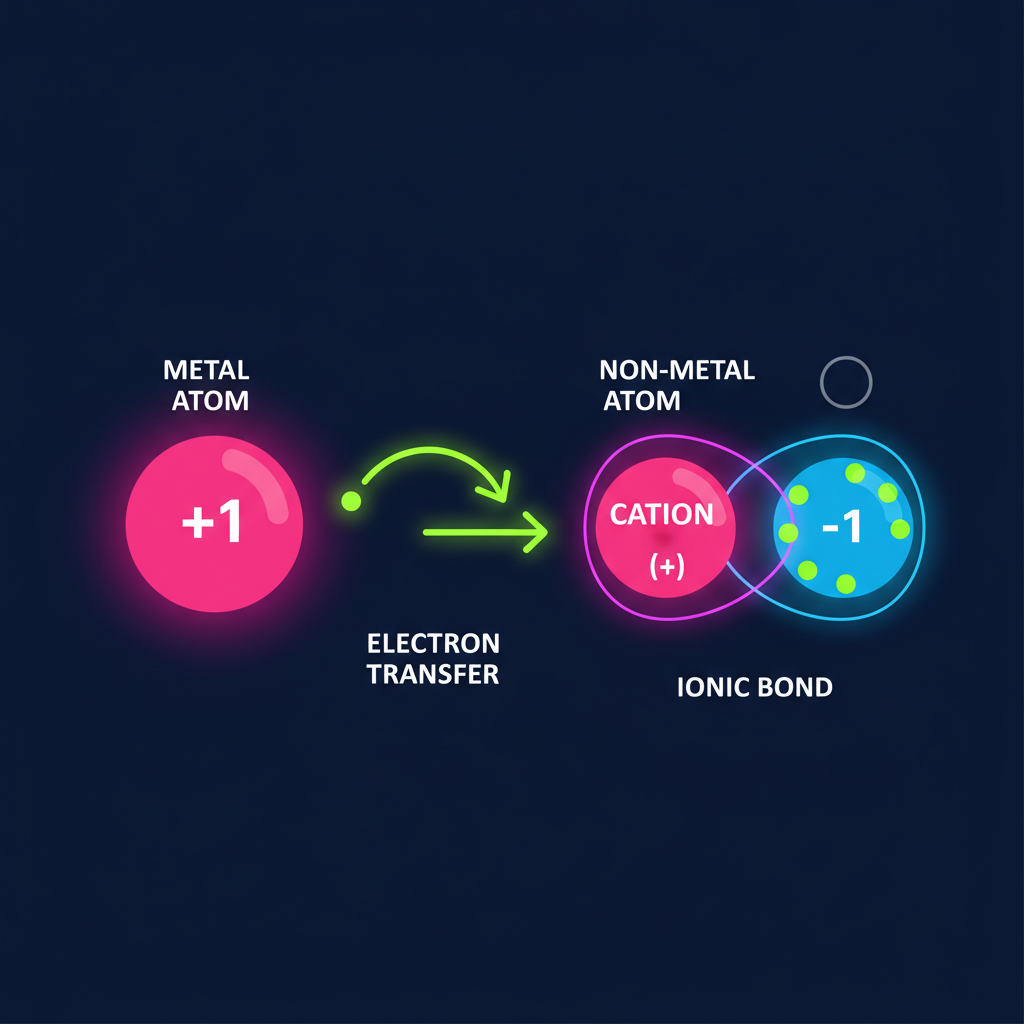
Salze sind chemische Verbindungen, die aus geladenen Teilchen (Ionen) bestehen. Sie entstehen meist aus der Reaktion eines Metalls mit einem Nichtmetall.
Kation (+): Meist das Metall (z.B. Natrium Na⁺)
Anion (-): Meist das Nichtmetall (z.B. Chlorid Cl⁻)
Das Ionengitter
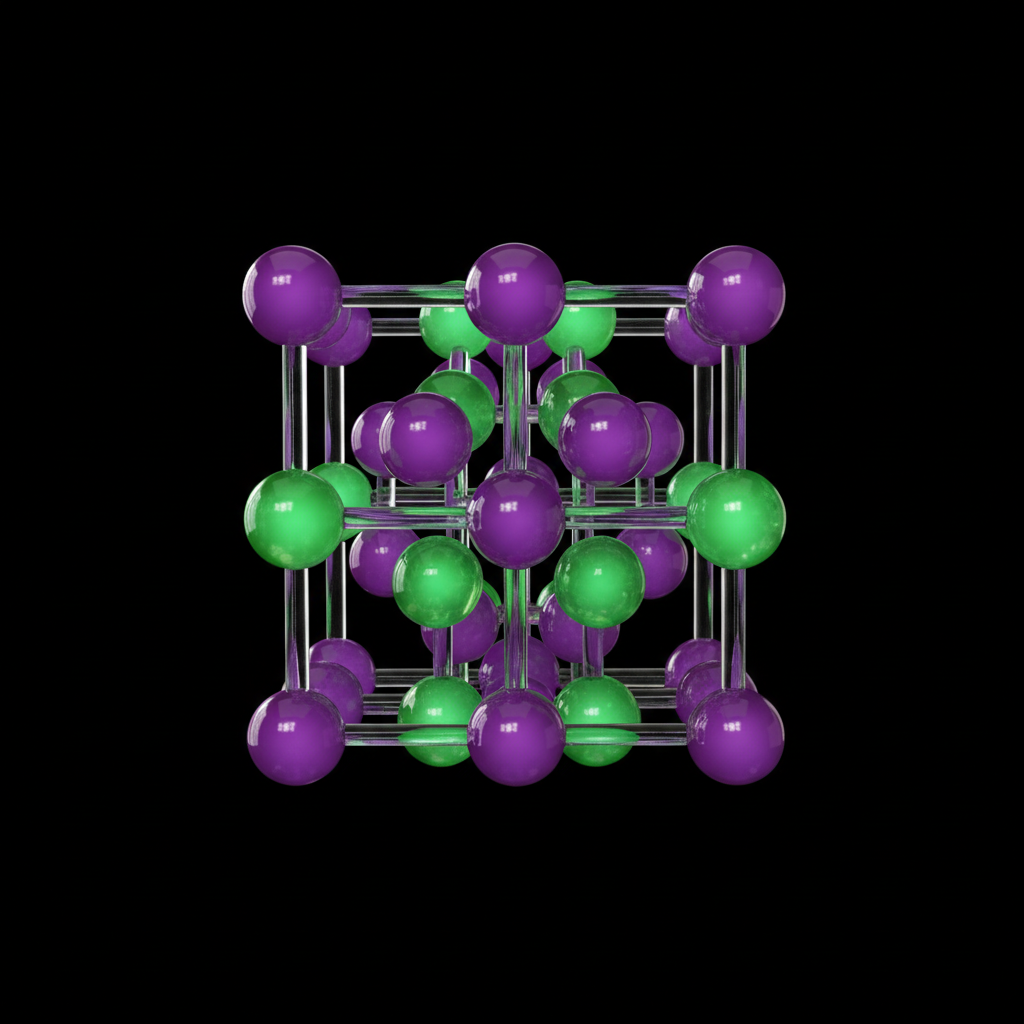
Salze bilden keine einzelnen Moleküle, sondern riesige, regelmäßige Gitterstrukturen. Positiv und negativ ziehen sich in alle Richtungen an.
Beispiel: Natriumchlorid-Gitter (Würfelform)
Eigenschaft: Hohe Schmelztemperaturen
Die Anziehungskräfte im Ionengitter sind extrem stark. Deshalb benötigen Salze sehr viel Energie, um zu schmelzen – ein klarer Unterschied zu Zucker oder Eis.
Elektrische Leitfähigkeit
⚡ Festes Salz: Ionen sind fest im Gitter eingesperrt. Kein Stromfluss (Isolator).
💡 Gelöstes Salz (in Wasser) oder Schmelze: Das Gitter bricht auf. Die Ionen sind frei beweglich und transportieren Ladung. Die Lampe leuchtet!
Herstellung: Die Neutralisation
Eine der wichtigsten Reaktionen der Chemie: Säure trifft auf Lauge.
Säure + Lauge → Salz + Wasser
HCl + NaOH → NaCl + H₂O
Fällungsreaktion: Wenn es schneit
Mischst man zwei klare Salzlösungen, kann ein schwerlösliches Salz entstehen. Es fällt als Feststoff aus.
Natriumchlorid (NaCl)
Bekannt als Kochsalz.
🍳 Würzen und Konservieren von Lebensmitteln
❄️ Streusalz im Winter (senkt den Gefrierpunkt)
🏭 Rohstoff für die Herstellung von Chlor und Natronlauge
Calciumcarbonat (CaCO₃)
Kommt in der Natur als Kalkstein, Kreide oder Marmor vor.
Problem Wasserhärte: Gelöste Calcium-Ionen bilden beim Erhitzen Kesselstein (Kalkablagerungen).
Kupfersulfat (CuSO₄)
Bekannt für die wunderschönen, tiefblauen Kristalle.
Chemischer Trick: Wasserfreies Kupfersulfat ist weiß. Kommt Wasser dazu, wird es blau → Nachweis für Wasser!
Zusammenfassung für die 1
Salze bestehen aus Ionen (Metall-Kation + Nichtmetall-Anion) in einem Gitter.
Sie haben hohe Schmelzpunkte, sind spröde und leiten Strom nur gelöst/geschmolzen.
Neutralisation: Säure + Lauge → Salz + Wasser.
Wichtige Salze: NaCl (Kochen), CaCO₃ (Kalk), CuSO₄ (Nachweis).
- chemie
- salze
- ionengitter
- neutralisation
- ionenbindung
- schulchemie
- lernen
- nacl