Biochimie de l'Œuf : Pourquoi le blanc change-t-il de texture ?
Découvrez les mécanismes moléculaires de dénaturation et coagulation des protéines de l'œuf lors de la cuisson, de l'état natif à la transition sol-gel.
Biochimie de l'Œuf : Pourquoi le blanc change-t-il de texture ?
Analyse moléculaire de la dénaturation et de la coagulation des protéines
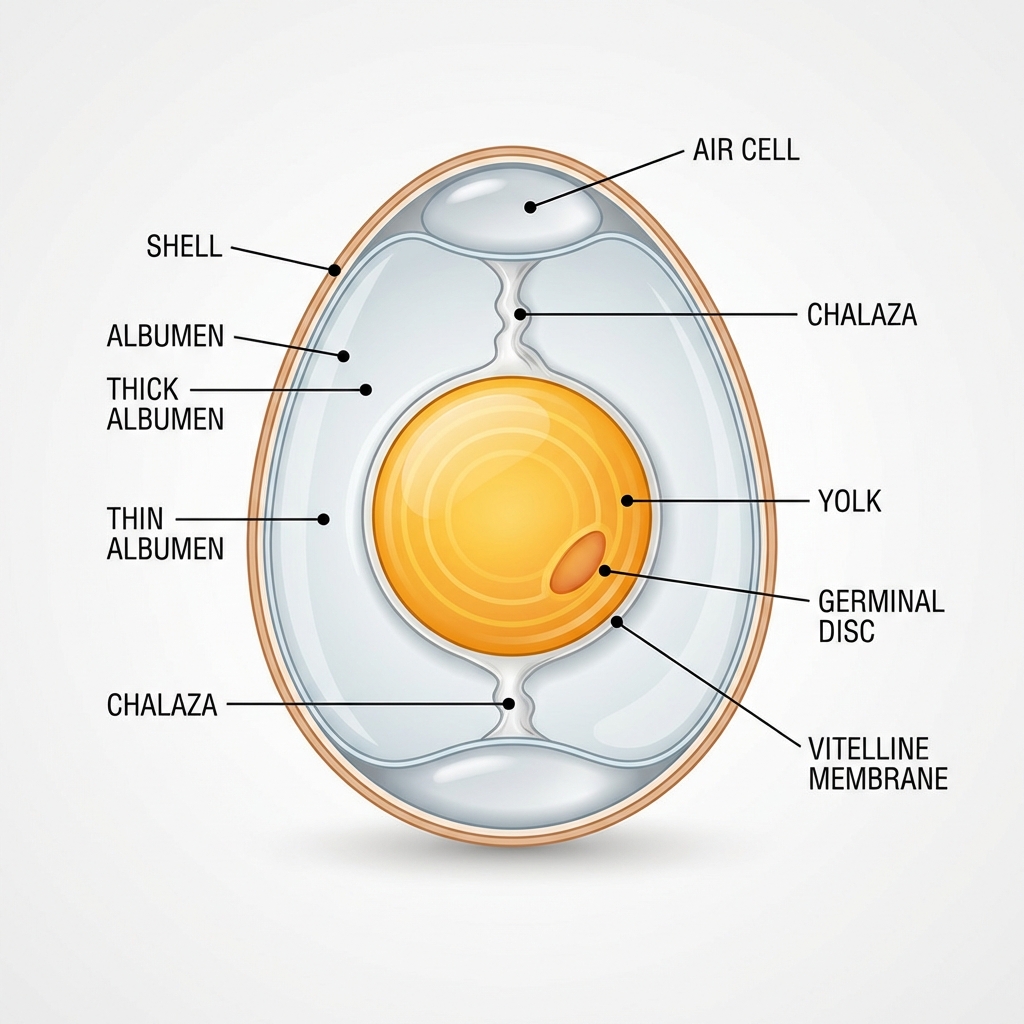
Anatomie Macroscopique et Constituants
Coquille : Carbonate de calcium, barrière physique perméable à l'air.
Albumen (Blanc) : Solution aqueuse de protéines globulaires (88% eau, 10-12% protéines).
Vitellus (Jaune) : Riche en lipides, cholestérol et protéines émulsifiantes (lécithine).
Chalazes et Membranes : Maintien structurel et barrière antimicrobienne.
Composition Biochimique de l'Albumen
Le blanc d'œuf est un système complexe dominé par l'ovalbumine. Ces protéines sont responsables des propriétés gélifiantes lors de la cuisson. Les sels minéraux jouent également un rôle dans la force ionique du milieu.
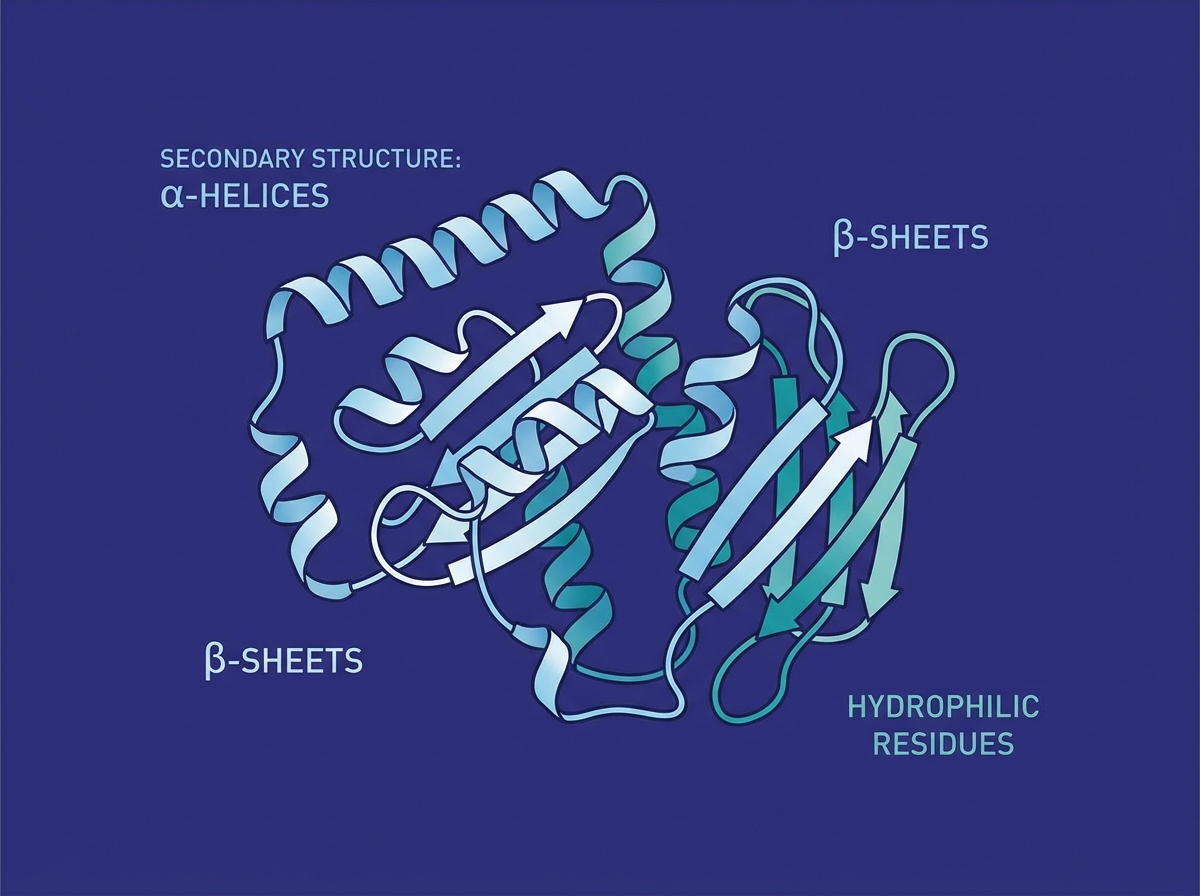
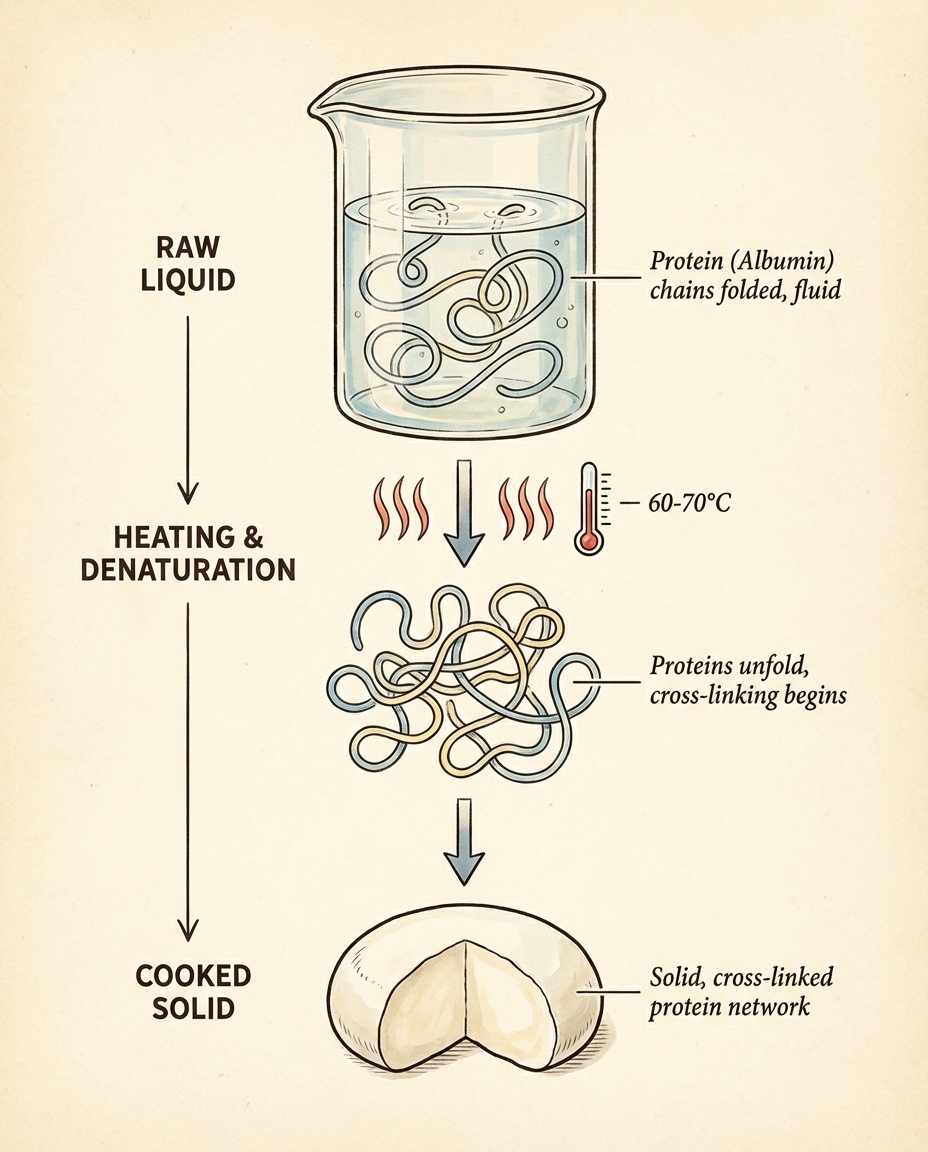
Structure Native des Protéines (Avant Cuisson)
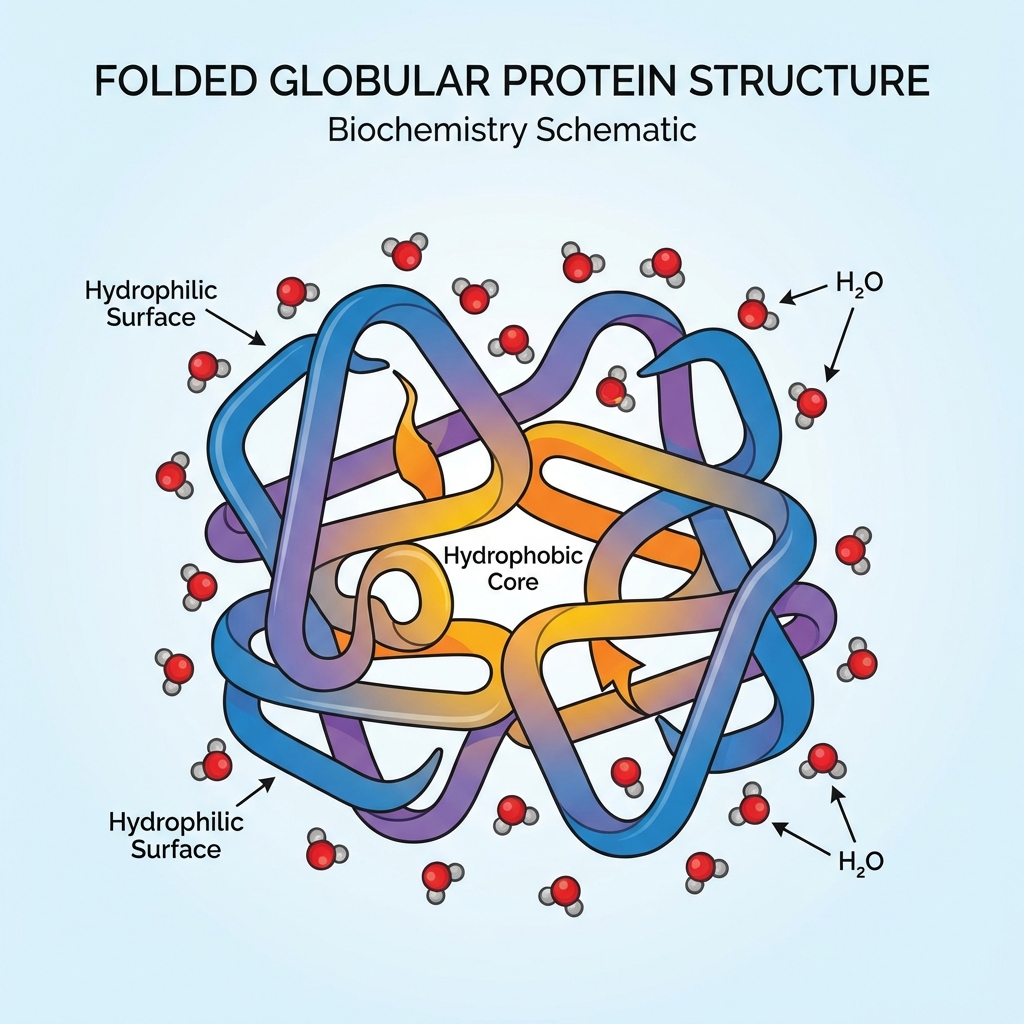
À l'état cru, les protéines comme l'ovalbumine sont globulaires et repliées sur elles-mêmes. • Structure tertiaire stable : Maintenue par des liaisons faibles (hydrogène, ioniques) et des ponts disulfure intramoléculaires. • Configuration : Les acides aminés hydrophobes sont enfouis au cœur de la protéine, loin de l'eau. • Les acides aminés hydrophiles sont exposés en surface, permettant la solubilité dans l'eau.
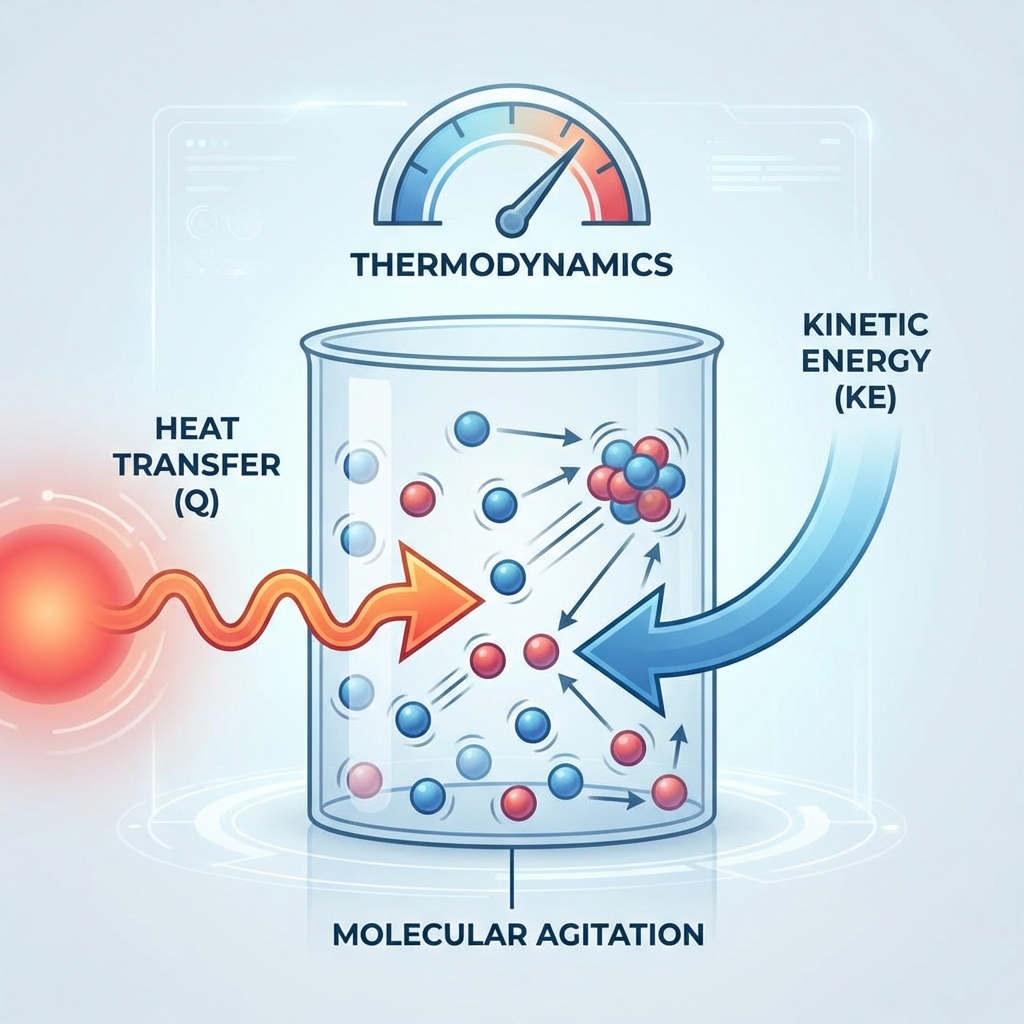
L'Apport d'Énergie : Thermodynamique de la Cuisson
Lors de la cuisson (pochage, omelette), l'apport de chaleur augmente l'énergie cinétique des molécules.
Montée en température (T > 60°C).
Agitation moléculaire violente.
Rupture des liaisons faibles stabilisant la structure native.
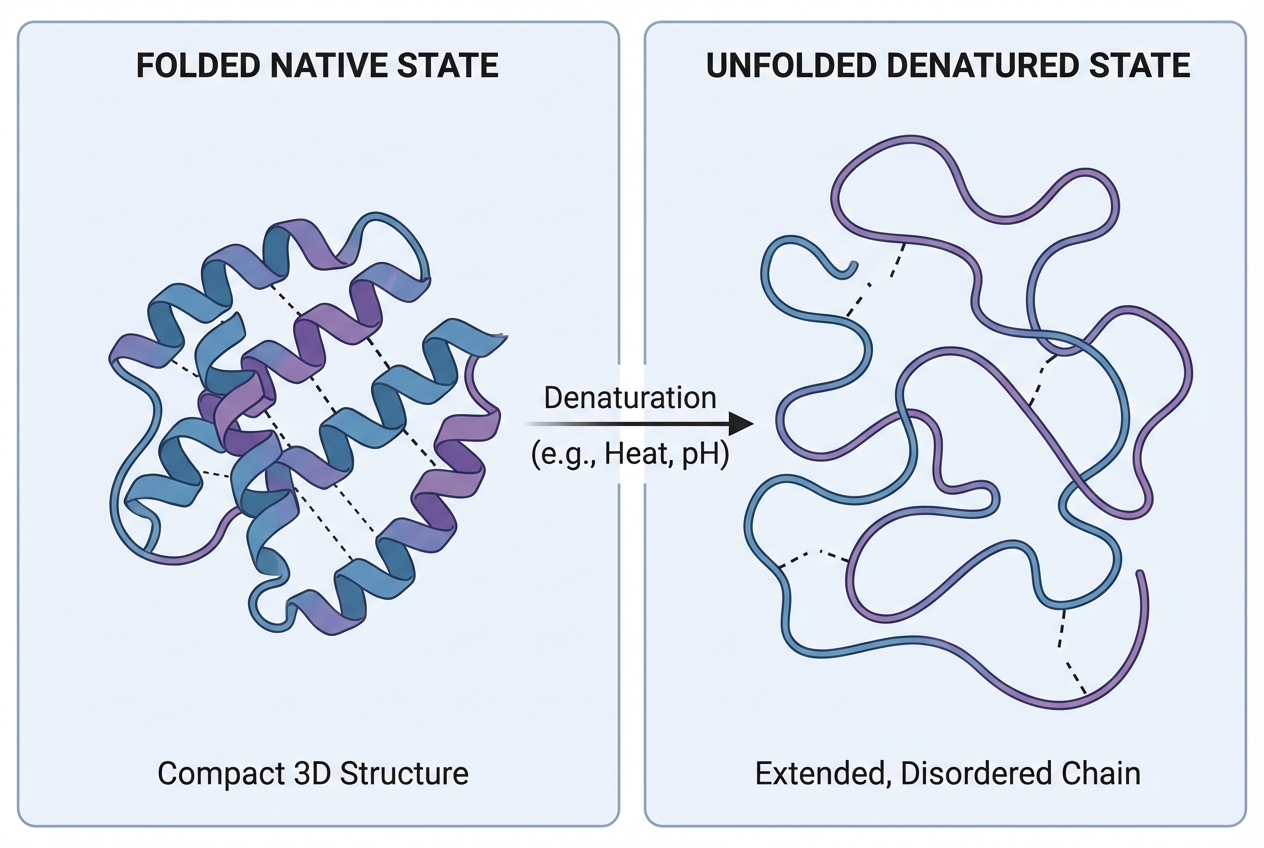
Mécanisme 1 : La Dénaturation (Déroulement)
Sous l'effet de la chaleur, la chaîne polypeptidique se déplie. C'est la perte de la structure tertiaire et quaternaire. La structure primaire (séquence d'acides aminés) reste intacte, car les liaisons peptidiques covalentes sont très fortes et résistent à ces températures.
Chimie des Liaisons : Ruptures
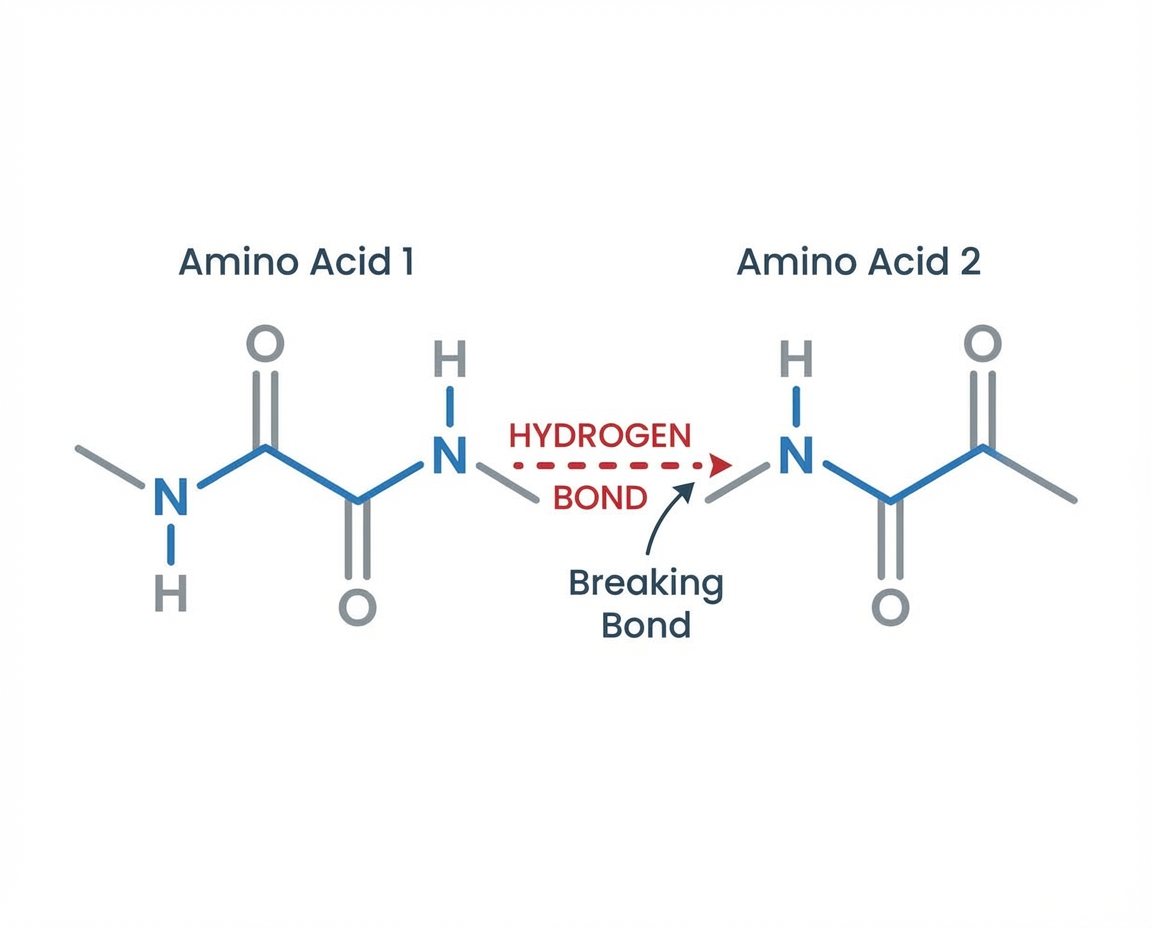
Liaisons Hydrogène
Forces faibles entre un atome d'hydrogène et un atome électronégatif (O, N). Elles sont les premières à céder sous l'agitation thermique.
Interactions de Van der Waals
Forces d'attraction à courte distance, stabilisant le cœur hydrophobe, perturbées par l'expansion de la molécule.
Mécanisme 2 : La Coagulation (Formation de Liaisons)
Une fois dépliées, les chaînes protéiques entrent en contact et forment de nouvelles liaisons intermoléculaires.
1. Interactions Hydrophobes : Les zones hydrophobes exposées cherchent à fuir l'eau et s'agrègent entre elles.
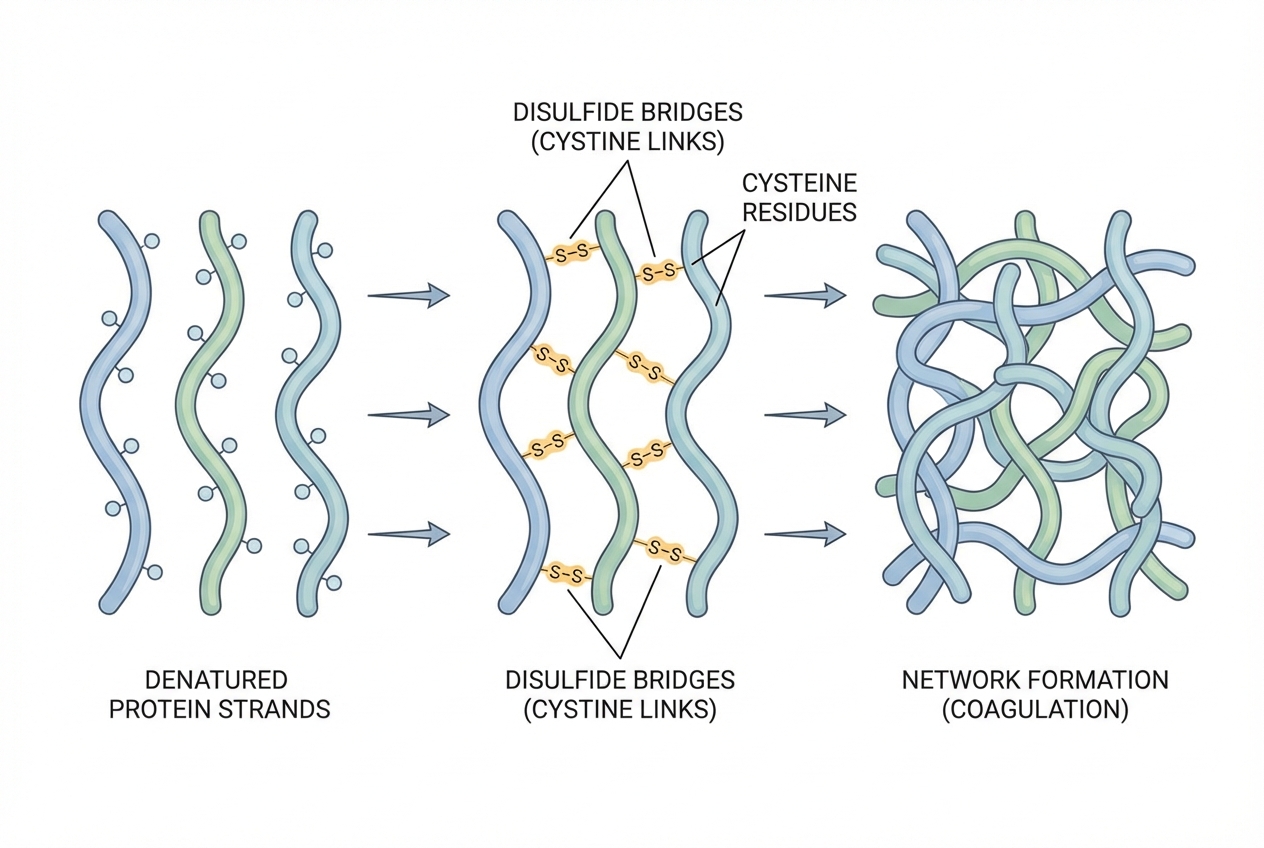
2. Ponts Disulfure (S-S) : Les acides aminés cystéine contiennent du soufre. Avec la chaleur, les groupes -SH forment des liaisons covalentes solides inter-chaînes.
Résultat Macroscopique : Transition Sol-Gel
Formation d'un Réseau Tridimensionnel : Les protéines agrégées piègent les molécules d'eau dans leurs mailles.
Solidification : Le liquide visqueux (sol) devient un semi-solide élastique (gel).
Opacité : Le réseau dense de protéines dévie la lumière (diffusion) au lieu de la laisser passer, le blanc devient... blanc.
Comparaison : Dénaturation Mécanique (Œufs battus)
Dénaturation sans chaleur (Omelette vs Meringue)
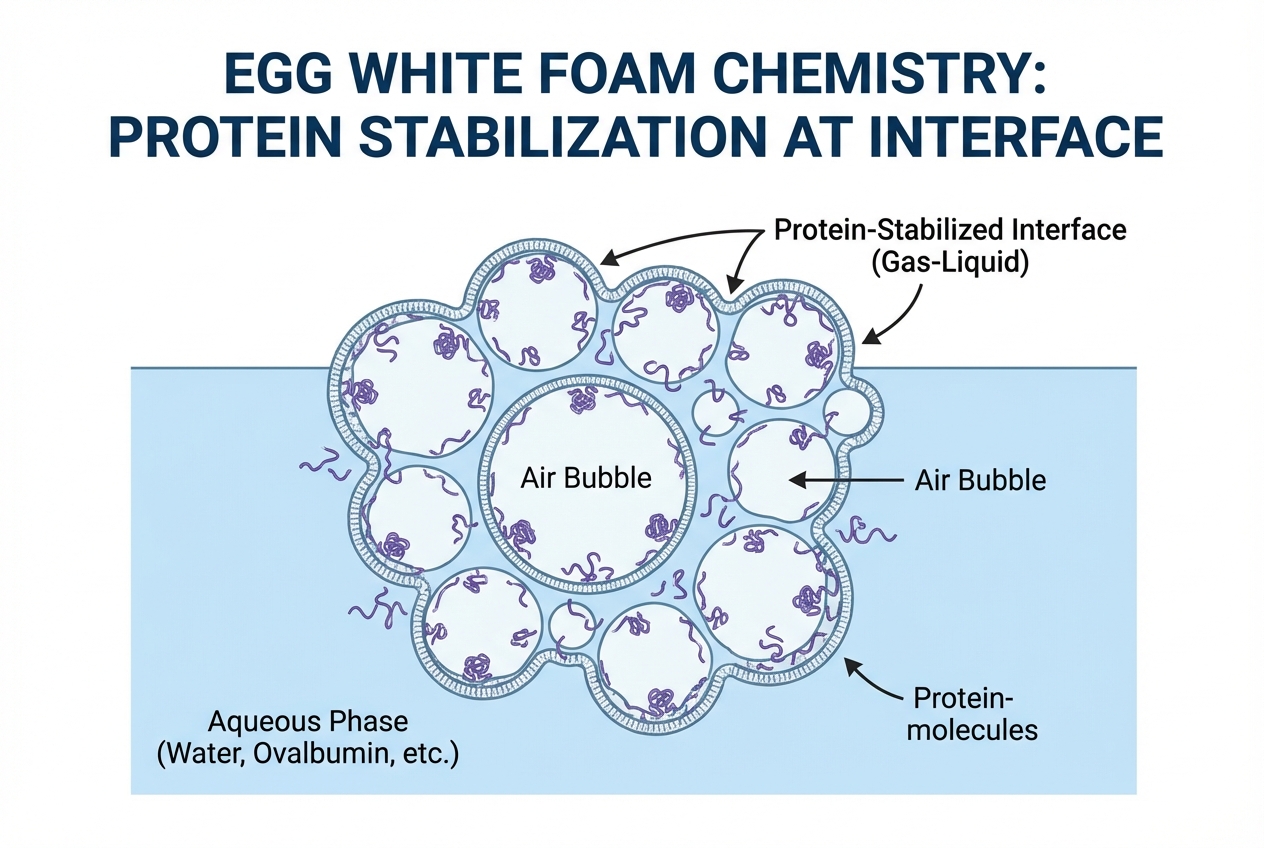
Action Physique : Le fouet introduit des bulles d'air et exerce un cisaillement.
Alignement à l'Interface : Les régions hydrophobes des protéines se placent vers l'air (intérieur de la bulle), les hydrophiles vers l'eau.
Résultat : Un film protéique rigide stabilise la mousse.
Synthèse Finale
La transformation de l'œuf est un processus irréversible de dénaturation et d'agrégation protéique. 1. État Natif : Protéines repliées, liaisons faibles. 2. Cuisson : Énergie cinétique rompt H-liaisons et Van der Waals. 3. Nouvelles Liaisons : Ponts disulfures et interactions hydrophobes créent un gel insoluble. 4. Résultat : Texture ferme, opaque et élastique.
- biochimie
- cuisine moléculaire
- protéines
- dénaturation
- coagulation
- théorie culinaire
- ovalbumine
- science